


胰岛素抵抗是肥胖及其相关代谢性疾病(如2型糖尿病、非酒精性脂肪肝和心血管疾病)的病理基础,而脂肪组织慢性低度炎症被认为是导致胰岛素抵抗的关键因素。在脂肪组织微环境中,除了巨噬细胞和T细胞等经典免疫细胞外,近年来发现的2型固有淋巴样细胞(ILC2s)在维持脂肪稳态、促进米色脂肪生成以及抑制局部炎症中发挥着重要作用【1-3】。已有研究表明,肥胖可导致脂肪组织中ILC2s功能受损,但其背后的分子机制尚不完全清楚。
mTORC1是细胞内重要的代谢调控枢纽,在免疫细胞发育分化和功能活化中起关键作用【4】。研究团队首先通过RNA-seq和磷酸化蛋白检测发现,高脂饮食(HFD)诱导的肥胖小鼠以及2型糖尿病患者的脂肪组织ILC2s中,mTORC1信号通路活性显著降低。机制探索表明肥胖小鼠血清中升高的游离脂肪酸(如棕榈酸)可直接抑制ILC2s中mTORC1的活化。为明确mTORC1在ILC2中的调控功能,团队构建了ILC谱系特异性(Id2-CreERT2)或ILC2特异性(R5/+)敲除mTORC1核心蛋白Raptor的小鼠模型。结果发现,Raptor缺失导致脂肪组织ILC2s数量减少、增殖能力下降、IL-5和IL-13等2型细胞因子产生受损。这表明mTORC1信号对维持ILC2的稳态和效应功能至关重要。
在机体代谢水平,ILC2特异性Raptor敲除小鼠在高脂饮食诱导下,虽体重和脂肪含量与对照组无显著差异,却表现出更严重的空腹高血糖、葡萄糖耐受不良和胰岛素抵抗。其脂肪组织中炎症性巨噬细胞(尤其是M1型)浸润增加,抗炎环境被破坏,形成了促胰岛素抵抗的微环境。过继转移实验进一步证实,来自Raptor敲除小鼠的ILC2s无法改善受体肥胖小鼠的糖代谢,凸显了mTORC1信号对ILC2代谢调节功能的必要性。 在细胞代谢水平,团队发现mTORC1缺失的ILC2s氧化磷酸化(OXPHOS)能力减弱,线粒体质量、ATP生成和备用呼吸容量均下降。RNA-seq提示线粒体生物合成相关基因(如Ppargc1a, Tfam)表达下调。这表明mTORC1通过调控线粒体代谢维持ILC2的适应性。深入机制研究发现mTORC1主要通过PPARγ调控ILC2线粒体代谢与效应功能。
已知PPARγ可调控IL-33受体ST2的表达【5】,本研究发现mTORC1-PPARγ轴确实调控ILC2s表面ST2的表达水平。Raptor缺失的ILC2 表面ST2表达下降导致ILC2对IL-33的反应性降低,而回补ST2同样能部分恢复Raptor缺失ILC2s的功能下降。这些结果表明mTORC1-PPARγ-ST2是一条连续的信号轴,共同维持ILC2的活化状态。上游机制研究表明,mTORC1通过促进低氧诱导因子-1α(HIF-1α)的表达来上调PPARγ。抑制HIF-1α可消除WT与KO ILC2s在PPARγ表达、线粒体质量及细胞功能上的差异。因此,mTORC1–HIF-1α–PPARγ构成了调控脂肪组织ILC2代谢与功能的核心信号通路。
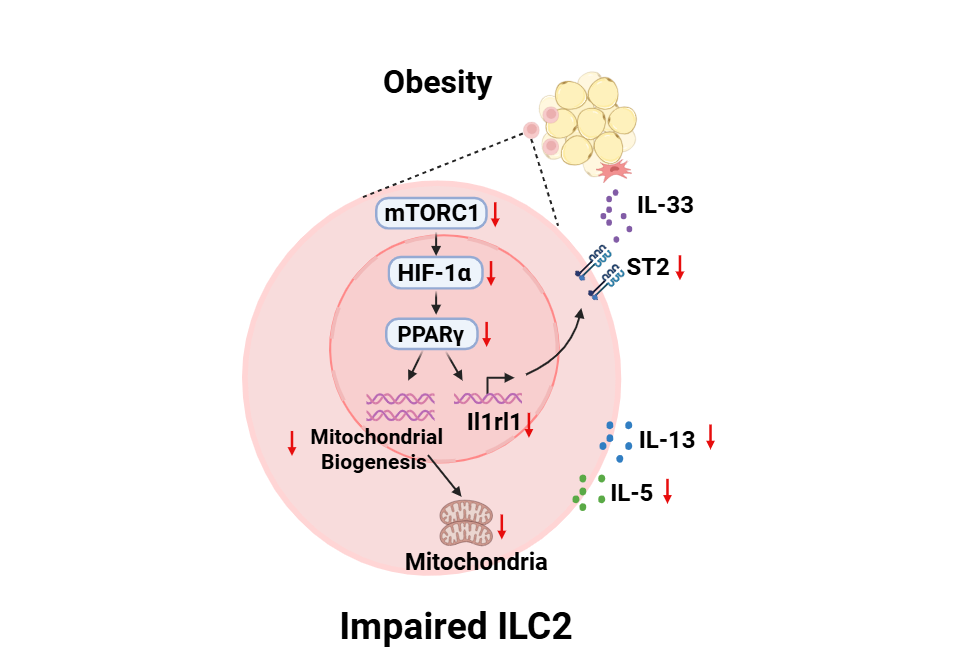
图1. 肥胖通过抑制mTORC1信号调控脂肪ILC2功能的作用机制模型
综上所述,本研究首次系统阐明了在肥胖状态下,脂肪组织微环境中的游离脂肪酸抑制ILC2s中mTORC1信号,进而通过HIF-1α–PPARγ轴损害其线粒体代谢、ST2表达及效应功能,最终导致脂肪组织炎症加剧和全身胰岛素抵抗的分子机制。该研究不仅深化了对肥胖相关免疫代谢紊乱的认识,也提示靶向脂肪组织ILC2的mTORC1-PPARγ通路,或通过改善ILC2代谢适应性,可能成为治疗肥胖相关2型糖尿病等代谢性疾病的新思路。
上海市免疫学研究所博士生胡琳和王冬娣为共同第一作者,沈蕾研究员和孙计萍副研究员为该论文共同通讯作者,中国科学院上海营养与健康研究所邱菊研究员和南京大学医学院附属鼓楼医院王洪东副研究员等在研究中提供了重要支持与帮助。
1. Stefan N & Cusi K. A global view of the interplay between non-alcoholic fatty liver disease and diabetes. Lancet Diabetes Endocrinol. 022;10:284-296.
2. Sun J, Zhang Y, Zhang Q, Hu L, Zhao L, Wang H, et al. Metabolic regulator LKB1 controls adipose tissue ILC2 PD-1 expression and mitochondrial homeostasis to prevent insulin resistance. Immunity. 2024;57.
3. Brestoff JR, Kim BS, Saenz SA, Stine RR, Monticelli LA, Sonnenberg GF, et al. Group 2 innate lymphoid cells promote beiging of white adipose tissue and limit obesity. Nature. 2015;519:242-246.
4. Tang J, Yang L, Guan F, Miller H, Camara NOS, James LK, et al. The role of Raptor in lymphocytes differentiation and function. Front Immunol. 2023;14:1146628.
5. Xiao Q, He J, Lei A, Xu H, Zhang L, Zhou P, et al. PPARγ enhances ILC2 function during allergic airway inflammation via transcription regulation of ST2. Mucosal Immunol. 2021;14:468-478.

沈蕾,研究员,博士生导师, 上海交通大学医学院上海市免疫学研究所课题组长,研究方向聚焦固有淋巴样细胞与疾病,近年工作以最后通讯作者身份发表在Nature Communications (2025), Immunity (2024), Nature Immunology (2022), PNAS (2024,2022), Cell Reports (2024), Cellular & Molecular Immunology (2023)等国际学术期刊。
 沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn
沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn