


Ku70由XRCC6基因编码,通常与Ku80形成异二聚体,参与识别DNA双链断裂位点,起始非同源末端连接(NHEJ)通路修复断裂DNA1。除此之外,Ku70还参与端粒维持、细胞凋亡调控2;通过V(D)J重排影响免疫细胞发育;作为胞质DNA感受器,调控先天免疫中干扰素和促炎性细胞因子的产生3;以及促进T细胞激活,增强与衰老相关的自身免疫性疾病4。已知FOXP3复合体中有Ku70存在5,但其功能未知,特别是在不同类型的适应性免疫细胞中是否存在独立于其DNA修复的非经典功能尚不清楚。
研究团队发现,肺腺癌肿瘤组织相比癌旁组织,Ku70蛋白表达更高,并且Ku70在肺腺癌(LUAD)中的表达与患者的预后呈负相关;同时,肺腺癌的肿瘤浸润调节性T(Treg)细胞中Ku70表达比传统T(Tconv)细胞和CD8+ 细胞更高。通过构建Foxp3启动子调控的Ku70条件性敲除的小鼠模型,团队发现随着年龄的增长在Ku70敲除的小鼠中,多种组织中的Treg数量显著降低,在肺组织中尤其明显。在过继性转移性结肠炎模型中,Ku70缺失的Treg细胞不能逆转结肠炎的发展。在LLC和B16F10两种肺定植肿瘤模型中,特异性敲除Treg中Ku70的小鼠肿瘤定植受限,Treg细胞浸润减少,表明Treg中Ku70的缺陷增强了肺部抗肿瘤反应。这些结果提示DNA修复蛋白Ku70可直接调节Treg细胞功能并影响免疫稳态,尤其是肺脏的免疫稳态。
为了进一步阐明Ku70对人Treg细胞功能的影响,研究团队通过敲低人iTreg 细胞中Ku70的表达,发现Ku70的敲低改变了Treg 细胞中FOXP3、CD25、CTLA4等多种功能分子的表达,体外抑制实验表明Ku70的敲低显著损伤了Treg细胞抑制CD8+ T细胞增殖的能力,表明Ku70对人和小鼠Treg细胞功能的维持均起着至关重要的作用。
研究团队通过免疫共沉淀实验发现Ku70与FOXP3存在不依赖于DNA的直接相互作用,且通过Ku70的Ku核心区(351-500aa)与FOXP3的锌指区(190-238aa)相互作用。肿瘤浸润性Treg细胞的RNA-seq分析揭示包括Tnfrsf19在内多个FOXP3靶向调控的基因表达改变,ChIP-seq分析表明FOXP3和Ku70在小鼠Treg细胞中共享大量靶基因。通过荧光素酶报告实验和ChIP-qPCR实验,进一步证明了人Treg细胞中Ku70特异性地结合FOXP3占据的染色质位点,并影响FOXP3的转录活性。
综上,研究团队揭示了Ku70独立于NHEJ的非经典功能,即DNA修复蛋白Ku70结合Treg细胞的核心转录因子FOXP3,维持FOXP3的转录调节能力,支持Treg细胞的免疫抑制功能,揭示了Ku70在免疫调节中的关键作用。在Treg细胞中Ku70的缺陷会抑制肺肿瘤的生长,促进抗肿瘤免疫,表明靶向Ku70不仅可以影响肿瘤细胞增殖,还能调控肿瘤免疫,实现对肿瘤的双重控制,从全新的角度解析DNA修复通路对免疫调控的影响,并为临床抗肿瘤免疫治疗提供了新思路。
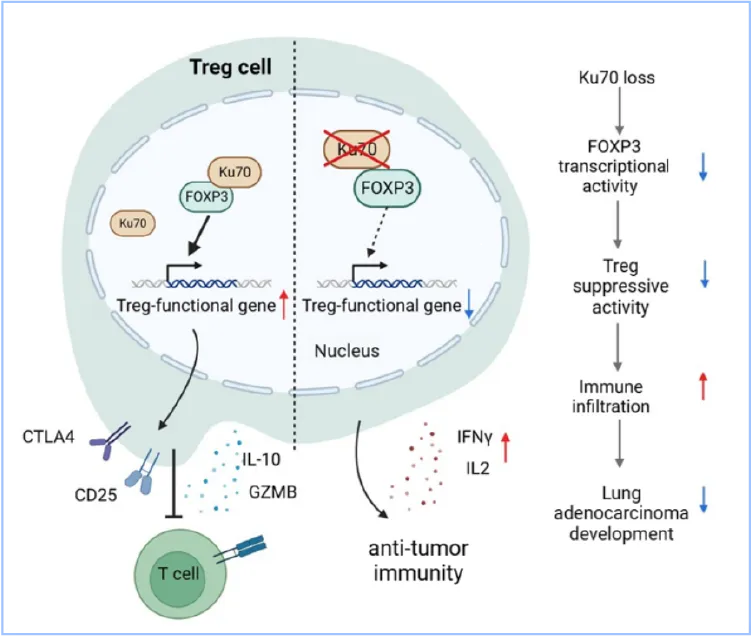
图1. Ku70结合Treg细胞核心转录因子FOXP3,维持其转录调节能力,支持Treg细胞免疫抑制功能
上海交通大学医学院上海市免疫学研究所博士生黄倩茹,上海交通大学医学院附属第六人民医院博士生田娜,上海交通大学医学院附属胸科医院硕士生章剑锋,以及上海交通大学医学院上海市免疫学研究所博士生宋诗阳为本文的共同第一作者。上海交通大学附属仁济医院汪川医师,芬兰奥卢大学生化与分子医学学院陈志教授,上海交通大学医学院附属胸科医院周谦君主任医师,以及上海交通大学医学院上海市免疫学研究所李斌研究员为本文通讯作者。本研究得到国家科技部重点研发项目、国家自然科学基金委重点基金、上海市科委等项目资助,依托上海市免疫学研究所公共平台、上海交通大学医学院基础医学院公共技术平台、上海交通大学医学院动科部、上海交通大学高性能计算中心、赛业生物动科部等平台的技术支持。本研究还得到了上海交通大学医学院上海市免疫学研究所叶幼琼研究员等老师和同学指导与帮助。
文章链接:
https://www.jci.org/in-press-preview
【参考文献】
1. Walker JR, Corpina RA, Goldberg J. Structure of the Ku heterodimer bound to DNA and its implications for double-strand break repair. Nature. Aug 9 2001;412(6847):607-14.
2. Amsel AD, Rathaus M, Kronman N, Cohen HY. Regulation of the proapoptotic factor Bax by Ku70-dependent deubiquitylation. Proc Natl Acad Sci U S A. Apr 1 2008;105(13):5117-22.
3. Zhang X, Brann TW, Zhou M, et al. Cutting edge: Ku70 is a novel cytosolic DNA sensor that induces type III rather than type I IFN. J Immunol. Apr 15 2011;186(8):4541-5.
4. Wang Y, Fu Z, Li X, et al. Cytoplasmic DNA sensing by KU complex in aged CD4(+) T cell potentiates T cell activation and aging-related autoimmune inflammation. Immunity. Apr 13 2021;54(4):632-647 e9.
5. Li B, Greene MI. Special regulatory T-cell review: FOXP3 biochemistry in
regulatory T cells--how diverse signals regulate suppression. Immunology. 2008
Jan;123(1):17-9.

李斌教授,二级研究员、余㵑(Hè) 学者、上海交大特聘教授、国家基金委免疫学杰青、上海市领军人才、上海市优秀学术带头人,上海市免疫学研究所科研副所长&课题组长、上海市欧美同学会副会长&生物医药分会会长、中国生物物理学会感染与免疫分会副会长、CBIITA联盟免疫治疗药物分会主任委员、PENN Medicine China Club 副会长;European Journal of Immunology执行副主编、CMI编委、JGG 编委等。
课 题 组 介 绍
李斌教授主要研究方向聚焦在FOXP3+调节性T细胞及其临床应用。先后承担国家基金委杰出青年基金、重点项目(3项)、移植免疫专项、中美及中波国际合作项目等。2009年回国以来,在国际一流学术期刊如Immunity、Nature Immunology、Nature Communications、PNAS等发表FOXP3+Treg领域一系列通讯及共同通讯作者论文一百余篇,H-index: 53,i10-index: 144。
博士后招聘要求
1、要求:
1)在国内外高校或研究所获得免疫学、分子生物学、细胞生物学、合成生物学等相关专业博士学位。应届毕业生优先考虑。年龄一般不超过35岁。
2)博士后申请人在国际高水平学术期刊上以第一作者/共同第一作者身份发表学术论文,以及在免疫治疗、CAR-T细胞构建、蛋白质结构解析等方向经验丰富者优先考虑。
3)具有良好的中英文阅读和写作能力。
4)具有良好的职业道德和团队协作精神,责任心强,身体健康。
2. 工作职责:
完成独立课题,协助PI指导研究生、管理实验室,参与申请基金等。
应聘材料及联系方式
有意者请将个人简历、2-3名推荐人联系方式以及应聘者认为重要的相关材料以电子邮件形式发送至binli@shsmu.edu.cn,邮件命名的格式:李斌课题组+博士后+姓名,应聘材料将予以严格保密。经审核合格的候选者我们将会邮件通知面试的具体时间、地点及其他相关事项。我们将根据申请者情况,按照上海交通大学医学院和上海市免疫学研究所有关政策,提供有竞争力的薪酬待遇,该广告长期有效。
 沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn
沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn