

TCR作为T细胞活化的第一信号通过识别抗原-MHC启动跨膜信号,触发位于CD3胞质段(cytoplasmic domain, CD3CD)的免疫受体酪氨酸激活基序(immunoreceptor tyrosine-based activation motifs, ITAMs)磷酸化,从而激活T细胞下游的系列反应介导特异性免疫应答。TCR/CD3复合体的信号机制一直是适应性免疫领域探索的核心科学问题,其中膜脂类物质作为细胞膜的主要成分可参与膜蛋白TCR/CD3复合体的信号调节。王锋团队前期发现CS可通过取代胆固醇破坏TCR的聚集并抑制TCR信号转导[1]。哈尔滨工业大学黄志伟课题组最近通过结构生物学技术证明CS与TCR的结合比胆固醇具有更强的竞争性[2]。中国科学院许琛琦课题组系列工作提出了TCR-CD3复合体变构模型[3、4],证明细胞膜内酸性磷脂(-)与CD3CD区域(+)通过电荷相互作用,将CD3亚基胞内段的ITAM锁定在细胞膜抑制TCR信号,而Ca2+刺激可破坏这种结合释放ITAM启动TCR信号传导。
该研究发现,带有负电硫酸基团的膜脂类分子CS可通过与带正电的CD3ε胞内段相互作用,形成稳定的二级结构锁定CD3ε胞质段与细胞膜的结合,由此防止Ca2+刺激下CD3ε-ITAM从细胞膜的释放,高效抑制TCR信号转导。通过进一步探索发现位于CD3ε-ITAM内的二级结构形成的关键位点(I191,YxxI-x6–8-YxxL),I191突变破坏了CS与CD3ε-ITAM形成的二级结构的稳定性,恢复并强化了CD3亚基对Ca2+的敏感性,从而显著增强TCR信号能力(图1)。重要的是,利用基因编辑技术在小鼠或人的TCR-T细胞引入CD3ε-I/A突变后,可以通过增加效应细胞因子分泌、增强肿瘤杀伤和提升肿瘤浸润T细胞干性扩增等多种途径,全面提升生理TCR-抗原亲和力范围内的各类TCR-T细胞的体内外抗肿瘤效力。该研究首次通过揭示TCR/CD3复合体信号调节机制,实现理性设计信号增强型TCR-T细胞的肿瘤免疫治疗策略,为日后进一步在临床上提升实体瘤免疫细胞疗效奠定了坚实的理论基础(图2)。
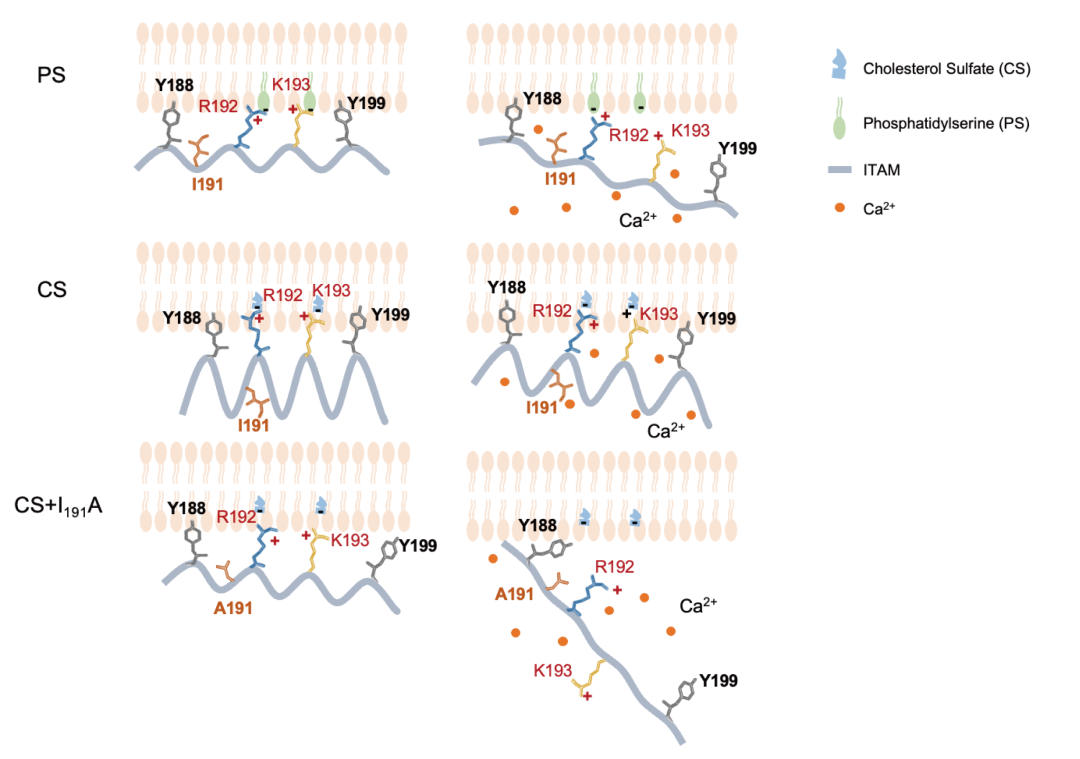
图1. CS通过影响CD3ε构象变化调控TCR信号新机制
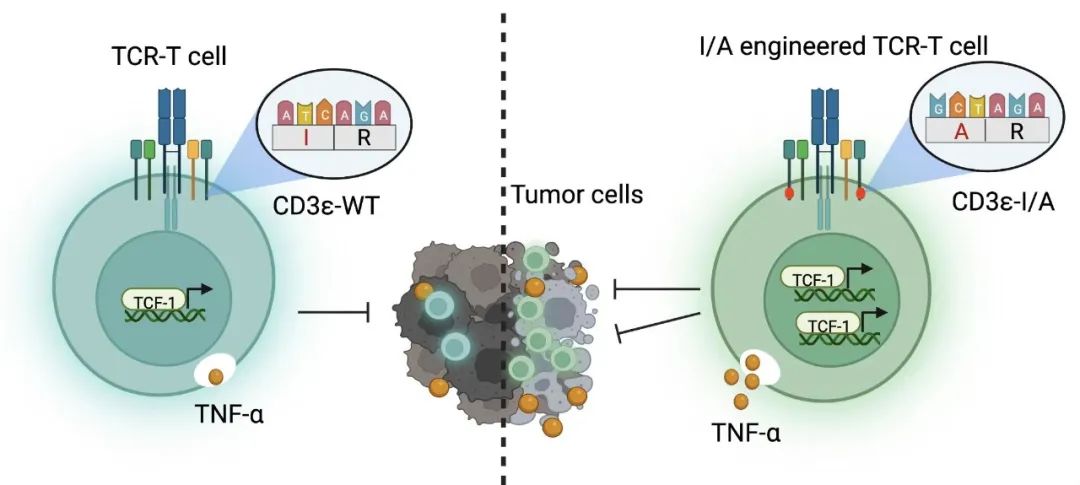
图2. CD3ε-ITAM I/A突变增强TCR-T细胞抗肿瘤效应
上海交通大学医学院上海市免疫学研究所王锋研究员为论文通讯作者,博士研究生梁文华,博士后蚁瑞荣(已出站),科研助理王为芳为论文的共同第一作者。研究还得到华东师范大学张楫钦博士和刘明耀教授等的大力支持。该研究工作受国家自然科学基金委员会,国家重点研发计划,上海市科学技术委员会,上海市地方高水平大学协同创新团队和医学基因组学国家重点实验室等经费支持。

王锋,研究员,博士生导师,上海交通大学医学院上海市免疫学研究所课题组长(PI)。2005年本科毕业于北京师范大学生命科学学院,2010年获得北京师范大学和北京生命科学研究所联合培养博士学位。2010-2016年在斯坦福大学师从T细胞受体发现者,美国国家科学院院士Mark M. Davis教授进行博士后训练。长期致力于T细胞抗原识别和信号转导的代谢调节机制研究。以通讯/第一作者在Nature Immunology(2016), PNAS(2018,2020), BMC Biology(2020),Cell Discovery(2021), Theranostics(2021),EMBO Journal(2022)等国际知名学术期刊发表系列研究论文。入选国家高层次青年拔尖人才,上海高校特聘教授(东方学者),上海市青年拔尖人才和浦江人才计划。近五年带领团队承担包括国家自然科学基金重点项目和国家重点研发计划在内的国家级课题11项,上海市科委和上海市卫健委资助的省部级项目4项。
王锋课题组近年来深入研究TCR抗原识别机制和抗原特异性T细胞在肿瘤等重大疾病中的作用,现根据课题组研究的需要,面向社会公开招聘,欢迎更多优秀人才加入团队共同推进课题进展,课题组将为加入的成员提供具有竞争力的待遇、一流的研究平台和良好的发展前景。相关申请事项请邮件联系:wangfeng16ATsjtu.edu.cn。
【参考文献】
1. Wang, F., et al., Inhibition of T cell receptor signaling by cholesterol sulfate, a naturally occurring derivative of membrane cholesterol. Nat Immunol, 2016. 17(7): p. 844-50.
2. Chen, Y., et al., Cholesterol inhibits TCR signaling by directly restricting TCR-CD3 core tunnel motility. Mol Cell, 2022. 82(7): p. 1278-1287.e5.
3. Xu, C., et al., Regulation of T cell receptor activation by dynamic membrane binding of the CD3epsilon cytoplasmic tyrosine-based motif. Cell, 2008. 135(4): p. 702-13.
4. Shi, X., et al., Ca2+ regulates T-cell receptor activation by modulating the charge property of lipids. Nature, 2013. 493(7430): p. 111-5.
 沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn
沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn