1


γδT细胞是一类主要存在于在粘膜组织中的T细胞亚群,在免疫监测、组织稳态及感染免疫等方面发挥重要作用。尽管γδT细胞和αβT细胞都起源于共同的胸腺T祖细胞,但有关γδT细胞发育和分化的调节机制仍知之甚少。N6-甲基腺嘌呤(N6-Methyladenosine, m6A)RNA修饰是存在于真核生物mRNA表观遗传修饰中的最普遍化学修饰之一,广泛参与机体的多种生理和病理过程。上海市免疫学研究所李华兵研究员团队致力于RNA表观遗传调控对免疫细胞发育、稳态和功能的研究,近年来陆续阐明了m6A在各类免疫细胞发育、稳态、分化和功能维持中的重要作用和分子机制1,2,3,4,5,6,但m6A修饰在胸腺T细胞早期发育和T细胞命运选择决定中的作用仍然未知。
本项研究中,研究团队发现胸腺T淋巴细胞中m6A去甲基酶ALKBH5缺失(ALKBH5fl/flLckCre)可特异性诱导γδT细胞的扩增,但并不影响αβT细胞的发育和功能,从而增强对胃肠道鼠伤寒沙门菌感染的保护。为了证明对小鼠伤寒沙门菌感染的保护来自于增加的γδT细胞,研究团队利用TCRδ-/-; ALKBH5fl/flLckCre小鼠模型删除γδT细胞而保留αβT细胞,结果显示保护作用消失。在ALKBH5fl/fl CD4Cre小鼠感染模型实验中也未发现敲除ALKBH5的αβT细胞能够起到保护作用,进一步排除了ALKBH5fl/flLckCre感染模型实验中ALKBH5在αβT细胞的功能。流式分析发现,ALKBH5fl/flLckCre小鼠胸腺T淋巴细胞中ALKBH5的缺失显著增加了双阴性(DN)阶段(特别是DN2和DN3阶段)中γδT前体各个亚群细胞的比例和数量。同时,体内BrdU实验揭示ALKBH5敲除自胚胎~E14.5时期开始即可显著促进γδT前体细胞的增殖能力。
Notch信号参与调节T淋巴细胞的发育和功能维持7,Notch受体与配体的相互作用参与了T淋巴细胞分化过程中细胞命运的决定8,9,10,11。在人类中,Jagged1主要诱导αβT细胞分化,而Jagged2介导的Notch3激活主要促进γδT细胞的发育,并通过阻碍TCRβ形成抑制αβT细胞的分化9。为了阐明m6A调控γδT细胞增殖的分子机制,研究团队结合先前T细胞中m6A-RIP-Seq数据,通过质谱分析、RNA-seq分析、m6A-RIP-PCR、RNA decay等实验,证实了ALKBH5缺失增加胸腺T前体细胞中m6A RNA修饰的丰度,并通过促进Notch信号关键靶基因Jagged1和Notch2 mRNA的降解来促进γδT前体细胞的增殖(见图1)。随后,研究团队进一步构建了Jagged1fl/flLckCre小鼠模型,验证了Jagged1信号缺失与ALKBH5敲除的表型一致,均促进γδT前体细胞的增殖,从而增加了成熟γδT的数量,进而可以更好的保护小鼠免受胃肠道鼠伤寒沙门菌的感染。
综上,该研究表明ALKBH5介导的m6A mRNA修饰通过调节Jagged1/Notch2信号通路在胸腺T细胞早期发育和T细胞命运选择决定中发挥了重要的检查点作用,加深了我们对m6A在特定微环境和免疫细胞中生理学功能的理解,揭示了前体T细胞早期发育过程中的RNA表观遗传学调控机制。
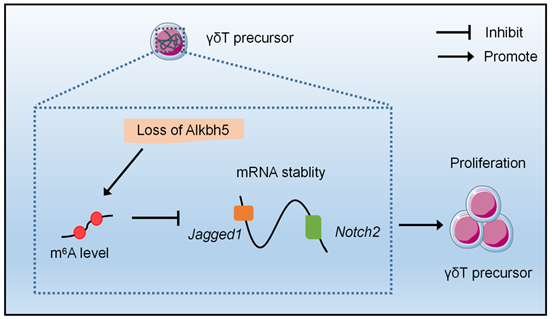
图1.m6A/ALKBH5通过靶向调控Jagged1/Notch2信号通路,在γδT细胞早期发育中发挥重要调控作用
上海交通大学医学院上海市免疫学研究所博士后丁陈波和余志斌,及耶鲁大学医学院博士生徐昊为本论文的共同第一作者,上海交通大学医学院-上海市免疫学研究所李华兵研究员、耶鲁大学医学院Richard Flavell院士、上海交通大学医学院附属瑞金医院胡伟国教授为该文的共同通讯作者。该研究得到国家自然科学基金重点项目、面上项目以及科技部国家重点研发计划等项目的资助。

李华兵,研究员,博士生导师。2002年本科毕业于南开大学并于2005年获得南开大学硕士学位,2011年在新泽西州立大学获得博士学位,2017年在耶鲁大学完成博士后研究。2017年8月正式入职上海交通大学医学院上海市免疫学研究所担任课题组长,建立RNA表观免疫课题组。最近五年的相关研究成果以通讯(含共同通讯)作者发表在国际权威杂志Nature Immunology、PNAS、Cell Research、Science Advances(3篇)、Nature Communications、Molecular Cancer和Nature、Immunity、Cell Reports等一系列杂志上。作为项目负责人主持国家自然科学基金委国际合作与交流项目(2021)、重点项目(2020)、面上项目(2020)、重大研究计划培育项目(2017)、两项上海市“科技创新行动计划”项目(2020),获得科技部重点研发计划子课题资助,并入选国家高层次海外人才青年项目(2017)和上海市“东方学者”特聘教授等人才项目。
李华兵课题组近年来深入系统地研究RNA修饰如何调控免疫细胞的功能以及在肠道炎症和肿瘤发生发展中的作用,现根据课题研究的需要,课题组面向社会公开招聘,欢迎更多优秀的人才(包括博士后和技术员)加入团队共同推进课题进展,课题组将为拟加入的成员提供上海地区具有竞争力的待遇、一流的研究平台和良好的发展前景。课题组更多详情参考实验室网页:https://hua-binglilab.com/。
 沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn
沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn