2022年6月14日,上海交通大学医学院上海市免疫学研究所吴学锋课题组等在国际学术期刊Cell Reports在线发表题为 “Vps33B controls Treg cell suppressive function through inhibiting lysosomal nutrient sensing complex-mediated mTORC1 activation” 的研究论文,研究揭示了囊泡蛋白33B(Vps33B)在通过维持内体/溶酶体系统稳态来调控氨基酸信号依赖的mTORC1通路的激活和细胞代谢,从而维持调节性T细胞的抑制功能。

调节性T(Treg)细胞在维持免疫稳态和控制免疫耐受中不可或缺。但Treg细胞的免疫抑制作用,既能防御人体发生自身免疫性疾病,又能抑制抗肿瘤免疫促使肿瘤细胞发生免疫逃逸,间接促进肿瘤细胞的增殖。因此在抗肿瘤免疫中,如何降低Treg细胞的抑制功能非常关键。Treg细胞的抑制功能受到mTORC1通路的严密调控,mTORC1通路的抑制或过度激活均影响Treg细胞的稳定性和功能。Treg细胞中mTORC1的过度激活会促使糖酵解水平升高,这会导致Treg标志性分子Foxp3水平降低,增强Treg细胞的不稳定性并使其向效应T细胞转化,致使炎症条件下Treg细胞抑制功能的丧失,然而mTORC1激活的动态和负调控机制仍不清楚。真核细胞中高度有序的内溶酶体系统对于细胞营养感应至关重要。近年来多项研究表明Vps33B介导内体/溶酶体系统中的囊泡运输以及外泌体分泌,由此对肝脏、造血、肿瘤的发生发展产生影响,但该蛋白及其所调控的内体/溶酶体系统如何控制Treg细胞的稳态和功能仍未知。
本项研究表明,Vps33B特异性缺失导致Treg细胞抑制功能缺陷并出现效应型T细胞表型,Treg抑制功能缺乏会导致小鼠T细胞稳态紊乱和T细胞效应性增强,从而使小鼠抗肿瘤免疫增强。机制方面,Vps33B与位于晚期内体/溶酶体上的mTORC1招募、激活必备元件——溶酶体营养感应复合物(LYNUS)结合,促进晚期内体和溶酶体融合,清除含有LYNUS的晚期内体/溶酶体,从而抑制mTORC1的激活。Treg细胞中Vps33B的缺失导致内体溶酶体融合受阻,进而导致LYNUS积累,使得mTORC1过度激活、糖酵解代谢水平上调、Foxp3表达水平和免疫抑制功能下降。综上所述,Vps33B通过维持内体/溶酶体稳态来调控氨基酸信号依赖的mTORC1的激活和细胞代谢,从而维持Treg细胞的抑制功能。该研究揭示靶向Treg细胞中的Vps33B是临床上提高抗肿瘤免疫力的潜在治疗策略。
上海市免疫学研究所2017级直博生项鸿睿是本研究论文的第一作者,通讯作者为上海市免疫学研究所的吴学锋研究员、邹强研究员和上海交通大学基础医学院刘俊岭研究员。本研究得到国家重点研发计划干细胞及转化专项、国家自然科学基金、上海市科委项目、细胞分化与凋亡教育部重点实验室和上海市细胞稳态调控与疾病前沿科学研究基地等的支持,上海市免疫学研究所及上海交通大学医学院基础医学院公共技术平台和动物科学部提供支持。上海交通大学医学院附属瑞金医院王正廷副主任医师、上海交通大学基础医学院钟清研究员、上海市免疫学研究所叶幼琼研究员、陈磊研究员及课题组成员等提供帮助。
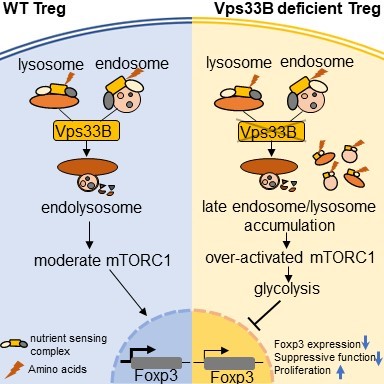
研究模型图:Vps33B缺失导致Treg细胞内体溶酶体融合受阻,进而促使溶酶体营养感应复合物 (LYNUS) 积累,mTORC1过度激活、糖酵解代谢水平上调、Foxp3表达和免疫抑制功能下降。
课题组简介:课题组长吴学锋,入选国家高层次人才计划青年项目。南开大学学士、硕士、美国宾州州立大学免疫学博士。美国德克萨斯大学M.D.安德森癌症中心、加州大学圣地亚哥分校博士后。加入上海交通大学医学院上海市免疫学研究所前在美国知名制药公司担任Senior Scientist,从事癌症免疫药物开发研究。课题组以开发治疗免疫疾病和癌症的药物和新策略为目标,聚焦连接炎症和肿瘤的细胞和分子机制,开展以下研究:1. 研究巨噬细胞和树突状细胞免疫代谢调控机制(European Journal of Immunology, 2022; Journal of Immunology, 2021; Theranostics, 2021);2. 探讨应激反应对T细胞和调节性T细胞代谢稳态和抗肿瘤免疫力的调控(Cell Reports, 2022; Nature Communications, 2021);3. 阐述肿瘤细胞来源的信号如何调控其微环境中的免疫细胞和免疫反应以探究肿瘤转移机制。课题组得到国家重点研发计划、国家自然科学基金、上海市科委项目等的经费支持,面向海内外招聘博士后,将提供上海地区具有竞争力的待遇、一流的研究平台和良好的发展前景。热忱欢迎青年才俊联系加入课题组。(实验室网页:https://www.shsmu.edu.cn/sii/info/1053/2087.htm;电子邮箱:xuefengwu@shsmu.edu.cn)。
课题组发表文章(2021年至今):
1.Hongrui Xiang, Yuexiao Tao, Zhenyan Jiang, Xian Huang, Huizi Wang, Wei Cao, Jia Li, Rui Ding, Mingyi Shen, Ru Feng, Linsen Li, Chenyang Guan, Jiamin Liu, Jun Ni, Lei Chen, Zhengting Wang, Youqiong Ye, Qing Zhong, Junling Liu,* Qiang Zou,* and Xuefeng Wu* Vps33B controls Treg cell suppressive function through inhibiting lysosomal nutrient sensing complex-mediated mTORC1 activation. Cell Reports (2022), https://doi.org/10.1016/j.celrep.2022.110943
2. Wang D#, Yuan T#, Liu J#, Wen Z, Shen Y, Tang J, Wang Z*, Wu X*. ATG16L2 inhibits NLRP3 inflammasome activation through promoting ATG5-12-16L1 complex assembly and autophagy. Eur J Immunol. 2022 Apr 15. doi: 10.1002/eji.202149764. PMID: 35426127
3. Kim MC#, Borcherding N#, Ahmed KK#, Voigt AP#, Vishwakarma A, Kolb R, Kluz PN, Pandey G, De U, Drashansky T, Helm EY, Zhang X, Gibson-Corley KN, Klesney-Tait J, Zhu Y, Lu J, Lu J, Huang X, Xiang H, Cheng J, Wang D, Wang Z, Tang J, Hu J, Wang Z, Liu H, Li M, Zhuang H, Avram D, Zhou D, Bacher R, Zheng SG, Wu X*, Zakharia Y*, Zhang W*. CD177 modulates the function and homeostasis of tumor-infiltrating regulatory T cells. Nat Commun. 2021; 12(1):5764. PMID: 34599187
4. Ni J, Guan C, Liu H, Huang X, Yue J, Xiang H, Jiang Z, Tao Y, Cao W, Liu J, Wang Z, Wang Y*, Wu X*. Ubc13 promotes K63-linked poly-ubiquitination of NLRP3 to activate inflammasome. Journal of Immunology 2021; 206(10):2376-2385. PMID: 33893171
5. Guan C, Huang X, Yue J, Xiang H, Shaheen S, Jiang Z, Tao Y, Tu J, Liu Z, Yao Y, Yang W, Hou Z, Liu J, Yang XD, Zou Q, Su B, Liu Z, Ni J*, Cheng J*, Wu X*. SIRT3-mediated deacetylation of NLRC4 promotes inflammasome activation. Theranostics 2021; 11(8):3981-3995. PMID: 33664876
原文链接:https://www.cell.com/cell-reports/fulltext/S2211-1247(22)00725-2
 沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn
沪公网安备 31009102000053号 沪ICP备18007527号-1 邮箱:sii@shsmu.edu.cn