北京时间3月4日凌晨, 国际学术期刊《自然》以Research Article形式在线发表了上海交通大学医学院上海市免疫学研究所苏冰教授课题组的研究工作。
该研究首次发现肠道干细胞底部存在一类被称为MRISC的新型肠道间质细胞,系统揭示了MRISC细胞在肠道炎症和损伤过程中通过特异调控肠道干细胞微环境的Rspo1-WNT信号参与肠道上皮组织损伤修复的作用和机理,为肠道修复和再生及疾病临床治疗研究提供了新思路。
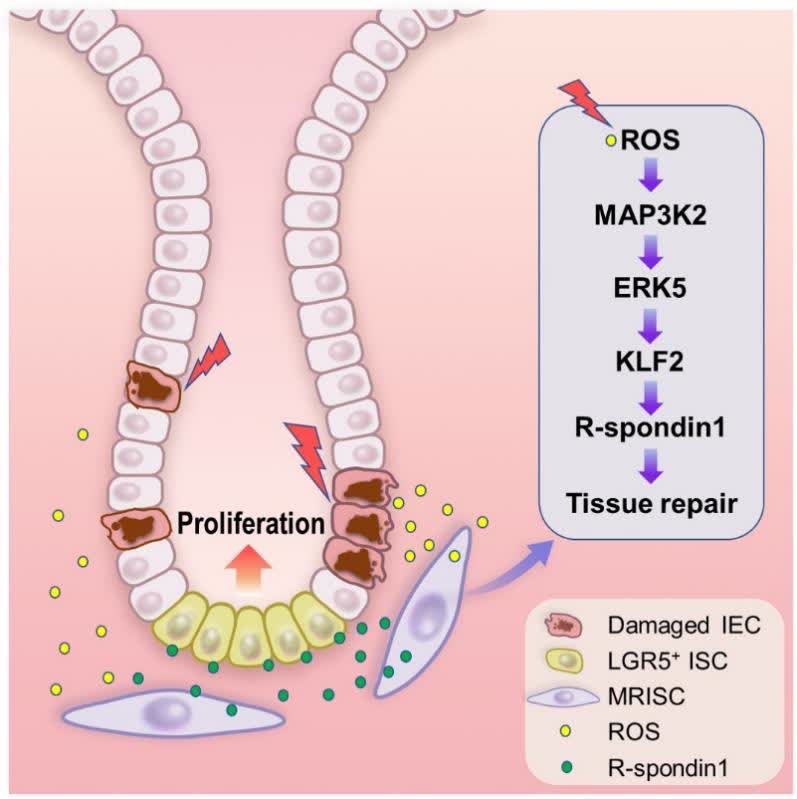
据悉,肠道间质细胞是肠道微环境组分中的重要成员。近年来单细胞测序技术快速发展,揭示了肠道间质细胞是一大类认知较少、异常复杂且具高度异质性的间质细胞。目前领域里对不同肠道间质细胞亚群的特征、空间分布、它们在组织损伤修复中的潜在功能、以及调节的细胞和分子机制仍知之甚少。因此对新型肠道间质细胞亚群的身份鉴定,上游刺激信号的发现,以及中下游转录和表观遗传调控通路的阐明已成为间质细胞领域最基础和重要的科学问题。
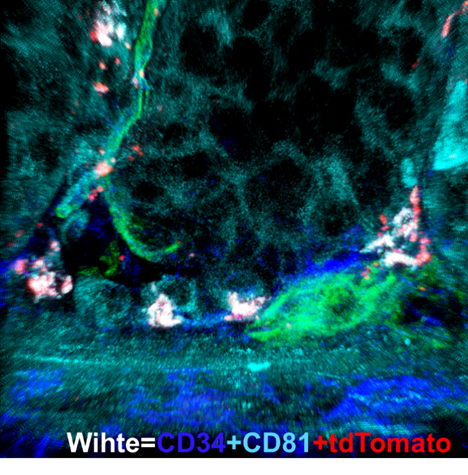
在苏冰教授课题组的研究中,研究人员利用单细胞测序技术发现并分离得到一群带有CD90+CD81+CD34+CD138-特征的肠道间质细胞,并命名为MRISC。通过肠道类器官共培养以及肠道原位细胞注射实验,课题组成功证明了MRISC具有对肠道干细胞特异的调节功能。并通过构建全新的Rspo1-tdTomato报告基因小鼠,揭示MRISC定位于肠道“干细胞巢”的下方。
在进一步的研究中,研究人员发现了MRISC有着与其他间质细胞非常不同的表观遗传调控特征,并且MRISC的核心转录调控因子KLF2直接受MAP3K2信号调控。后续的体外实验进一步发现了“活性氧(ROS)-MAP3K2-ERK5-KLF2”这一全新的诱导R-spondin1产生分子通路。通过同人肠道单细胞测序数据的比较分析,研究人员也找到了与小鼠MRISC对应的人的MRISC细胞,并猜测其同样可能参与调控肠道炎症。
MRISC以及其它主要间质细胞亚群标记系统的建立必将极大推动间质细胞在免疫、神经、肿瘤、代谢、衰老等生命科学重要过程中功能的阐释;而人体内相对应的间质细胞主要亚群的发现和鉴定将同样推动其在人类疾病如肠道肿瘤、食物过敏等炎症诱导疾病中作用的解析。
这项研究是苏冰教授团队通力协作的成果,也是苏冰教授离开耶鲁大学回国后加入上海交通大学医学院开展的第一个课题。课题组伍宁波博士和孙宏翔博士是该论文的共同第一作者。

苏冰教授是上海交通大学王宽诚讲席教授,上海市免疫学研究所所长,上海交通大学医学院免疫与微生物系系主任。苏冰教授同时兼任上海交大医学院-耶鲁大学免疫代谢联合研究院主任。苏冰教授长期致力于MAPK和SIN1/mTOR调控的细胞信号转导研究,取得了一系列突破性科学发现和成果。相关工作以通讯作者相继发表于国际顶尖杂志包括Cell,Nature Genetics,Nature,Nature Immunology,Immunity,EMBO J, Blood,Mol Cell等杂志。近年来苏冰教授课题组聚焦肠道黏膜免疫和炎症相关疾病的基础研究,并与瑞金医院、仁济医院等临床科室合作开展临床转化研究。
链接:https://wap.gmdaily.cn/article/434c0d3364e444b5978eaae27762e6f5?from=singlemessage
