病毒与人类的博弈是一场贯穿生命演化的漫长战争。病毒不断攻击人类引起多种疾病,同时人类免疫系统积极对抗,并逐渐将病毒序列整合入基因组,实现协同进化。内源性逆转录病毒(Endogenous Retrovirus, ERV)是数百万年前远古逆转录病毒入侵人类细胞后在染色体上留下的“化石”,约占人类基因组的8%,形成独特的基因印记。绝大多数ERV在表观遗传和基因擦除等机制的作用下处于沉默状态,是人类基因组中的“暗物质“,阐明其潜在的生理和病理学意义是生命科学的重大挑战。
心力衰竭(Heart Failure, HF)简称心衰是一类复杂的临床综合征,特征是心脏无法泵出足够的血液来满足机体的需要。现在全球心衰病人约有1.64亿人,由于缺乏有效的治疗,其5年死亡率超过50%,比大多数类型癌症的死亡率都要高,成为人类的主要杀手。

8月18日,上海交通大学张冰/孙锟/朱丹团队在Circulation杂志上发表题为An Aberrant Resurgence of Endogenous Retroviruses Prompts Myocarditis and Heart Failure的研究成果,首次发现内源性逆转录病毒特别是ERV1亚家族在多种类型心衰中复活,通过激活固有免疫Toll样受体TLR7/9进而导致心肌炎及心力衰竭。相反,抑制ERV复活或阻断其诱导的固有免疫过度激活可有效减轻心力衰竭。
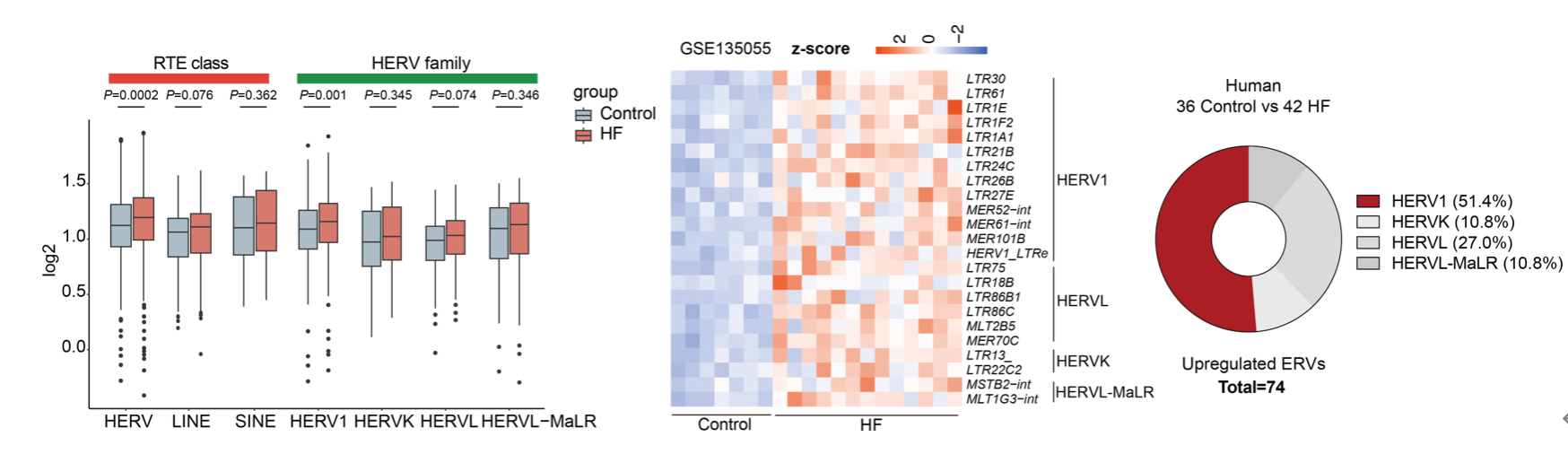
为探索ERV在心衰中的作用,作者首先构建了逆转座子RNA的分析方法,系统分析了78例已发表的扩张型心肌病(DCM)和缺血性心肌病(ICM)心衰患者在内的心室全RNA转录组数据集。结果发现在心衰心肌组织中ERV显著上调,而其他逆转座子如LINE,SINE等未见明显变化。其中ERV亚家族HERV1在三个数据集中一致且显著上调,是激活ERV中的主要亚型。作者还在小鼠及非人灵长类心衰模型中进一步证明ERV1亚家族也同样显著激活,表明ERV1激活是多类型心衰的共同分子特征。
表观遗传抑制是基因组ERV转录沉默的主要机制,该研究发现表观遗传抑制关键因子TRIM28在HF心肌样本中显著下调。为探究其在ERV和HF中的调控功能,作者构建了TRIM28诱导敲除的小鼠。 全RNA转录组分析显示TRIM28缺失导致心脏中ERV基因显著上调,其中ERV1占主导,荧光原位杂交进一步证实ERV1在心肌细胞胞质内呈斑点状增多,这与多种心衰模型中ERV的激活模式一致。TRIM28诱导敲除后出现严重的急性心衰表型:心功能急剧下降、心腔扩大、室壁变薄、心衰标志物显著升高,并伴随肺肝充血水肿。小鼠在敲除后4天就开始死亡。
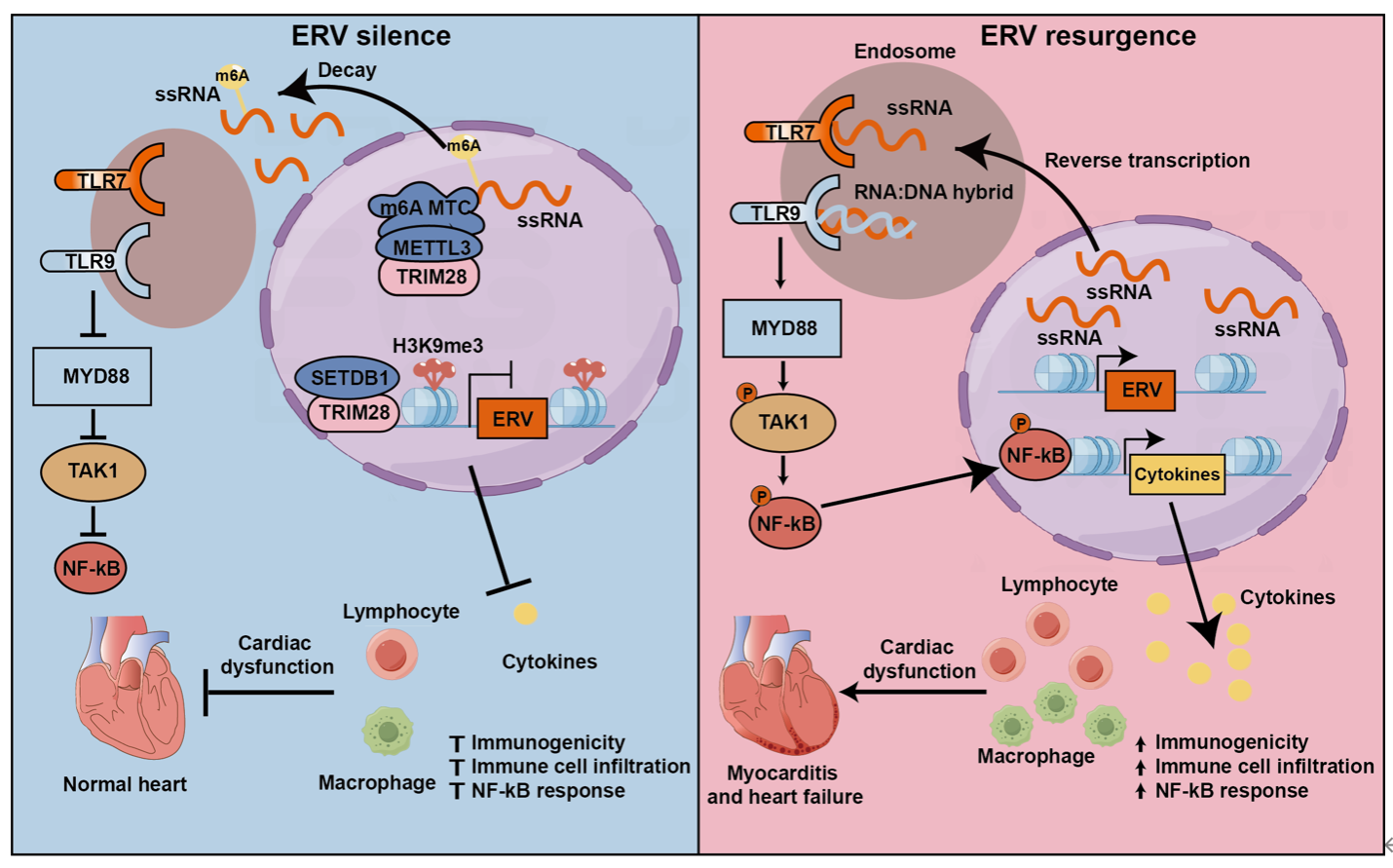
进一步的机制研究表明TRIM28通过双重表观遗传调控机制共同抑制ERV激活。一方面TRIM28通过组蛋白H3K9三甲基化(H3K9me3)抑制部分ERV激活;而对于H3K9me3非依赖的ERV,TRIM28则通过招募m6A甲基转移酶METTL3到ERV RNA,促进其m6A甲基化修饰和降解,进而抑制其表达。心肌细胞中激活的ERV触发了强烈的先天免疫反应,其RNA转录本或者逆转录出的DNA被Toll样受体TLR7/9识别,进而特异性激活NF-κB炎症通路和下游IL6, IL1b, TNFɑ等炎症因子的表达。有意思的是与外源性病毒通常通过固有免疫激活干扰素IFN通路不同,ERV升高在心肌细胞中并没有激活IRF-IFN通路,而只是特异性激活了NF-κB通路。 异常的固有免疫激活促进CD3+T细胞和CD68+巨噬细胞的浸润,导致心肌炎症和心肌细胞死亡,最终导致急性心衰。时序实验进一步发现ERV激活和炎症反应早于心衰标志物的表达,从而证实ERV激活是驱动心肌炎症和心衰的始动因素。针对上述致病机制,作者进行了干预研究。注射TLR7/9抑制剂NSC4375和NF-κB抑制剂JSH23显著提高了TRIM28iCKO小鼠的生存率,减轻了炎症浸润和纤维化,改善了心功能。使用逆转录酶抑制剂也取得了相似的心脏保护效果,进一步证明ERV是导致心肌炎和心衰的使动因素。急性HF(Acute HF, AHF)是HF中最为严重的亚型,包括突发型HF或原有HF的快速恶化,其1年期死亡率约为30%。心肌炎尤其是暴发性心肌炎,是AHF的常见潜在病因。心肌炎通常由外源性病毒包括逆转录病毒感染引起,如柯萨奇病毒B、腺病毒、疱疹病毒、HIV和SARS-CoV-2等。而本研究首次发现并证实内源性逆转录病毒激活也可以导致急性心肌炎和心衰。
缺血再灌注导致心衰是临床上常见的心衰类型。作者在缺血再灌注心衰模型(I/R)中也发现TRIM28-ERV-TLR7/9-NF-κB通路的显著激活,预示干预该通路可能会保护I/R导致的心衰。作者采用腺相关病毒AAV9在心肌组织内特异性恢复TRIM28能够有效抑制ERV激活,并阻断TLR7/9-NF-κB通路活化以及炎症因子表达。AAV9-TRIM28显著减小梗死面积,并改善心功能和心肌的病理重构。进一步采用TLR7/9抑制剂NSC4375抑制固有免疫也取得了相似的心肌保护效果。需要指出的是项目合作者——华中科技大学汪道文/陈琛团队以及其他研究团队在新冠疫情期间也曾采用TLR7/9抑制剂治疗新冠病毒感染引起的心肌炎和心力衰竭并取得了良好的治疗效果。这些研究都表明TLR7/9介导的固有免疫激活在心肌炎和心衰中关键致病作用。
综上,本研究首次发现并证实内源性逆转录病毒ERV特别是ERV1亚家族的激活是心衰的共同分子病理特征。本研究还首次揭示了一个全新的分子通路“TRIM28-ERV-TLR7/9-NF-κB“,并证明其在心肌炎和心衰中的关键作用。靶向该通路可能为心肌炎和心衰的治疗提供新的治疗靶点。
本研究得到了科技部、国家自然基金、上海市科委、上海教委和上海交通大学“星计划”等项目的支持。上海交通大学医学院附属新华医院张冰教授、孙锟教授以及胸科医院的朱丹教授为该文共同通讯作者,上海交通大学系统生物医学研究院博士生熊俊浩、助理研究员张沙沙、博士生耿子龙和硕士生林珺涛为该文共同第一作者。该工作得到了复旦大学中山医院孙爱军教授、第三军医大学的吴庚泽和曾春雨教授、华中科技大学陈琛和汪道文教授、上海交通大学生物医学工程学院张岩教授,上海交通大学医学院陈丰原、侯旭敏和李若谷教授、温州医科大学郭晓令研究员、南方科技大学冯宇亮研究员、香港中文大学田小雨教授、中国科学院广州生物医药与健康研究院陈捷凯研究员以及北京大学伊成器教授的合作支持。
