多样化病理基础大模型的涌现,提升了各类计算病理学任务的性能。然而,由于模型架构和预训练数据来源的差异,不同模型在下游任务中表现各异、各具优势,从而增加了模型选择的复杂度。此外,由于病理图像数据具有隐私性强等特点,汇总多源数据以重新训练病理基础模型在实践中难以实现。

近日,医学院临床医学研究院俞章盛教授团队提出了Meta-Encoder方法,为解决这一问题提供了有效方案。该研究成果发表于Nature Communications,临床医学研究院高瑞恬博士为该论文第一作者,已毕业硕士研究生杨钊昌为共同第一作者,俞章盛教授为通讯作者。
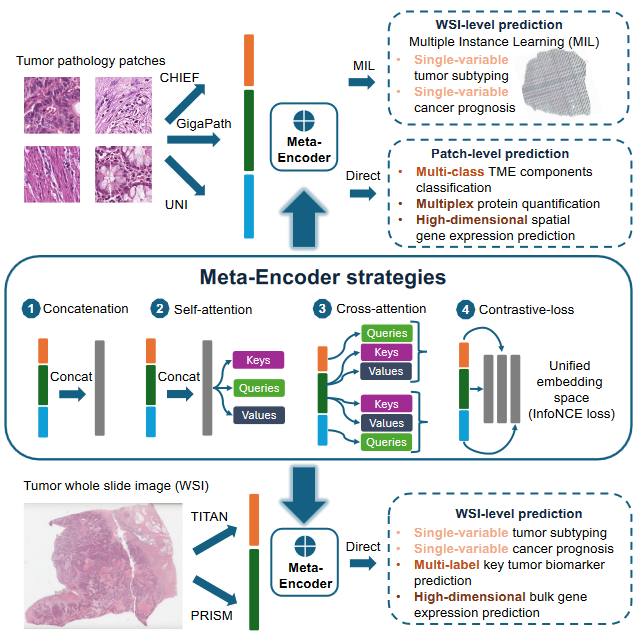
针对上述挑战,研究人员提出的Meta-Encoder方法,通过整合多个病理基础模型,增强对病理图像的表征能力,进而提升下游任务的预测精度,为精准肿瘤学的发展提供支持。实验结果表明,Meta-Encoder能有效融合多个在异构数据集上预训练的基础模型,充分发挥其互补优势。针对基于病理图像的肿瘤亚型分类等简单任务,Meta-Encoder拼接策略可匹敌甚至超越最佳单个模型性能,有效规避模型选择偏差;对于癌症关键生物标记物及空间组学表达预测等复杂任务,Meta-Encoder自注意力策略表现尤为突出,显著优于最佳单个模型。值得一提的是,Meta-Encoder方法在图像特征层面实现轻量级集成,无需接触原始训练数据,计算效率高,并具有良好的可扩展性,便于集成新出现的基础模型。
该创新性方法不仅有效缓解了病理基础模型选择难、病理图像数据共享难的现实困境,也为充分挖掘已有模型潜力、推动多模型协同应用提供了全新思路。未来,该框架有望进一步整合更多样化的预训练模型与多模态数据,持续赋能精准肿瘤学的临床转化与智能病理诊断的发展。
