近日,国际著名学术期刊Cell Death and Differentiation在线发表了基础医学院解剖学与组织胚胎学系最新研究成果“Intracellular ASIC1a regulates mitochondrial permeability transition-dependent neuronal death”。该项研究揭示了酸敏感离子通道1a亚型(ASIC1a)介导中枢神经元死亡新机制,由博士后王宜之及其合作者在徐天乐教授指导下完成。
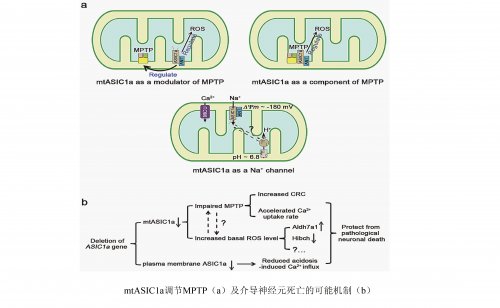
神经元死亡和神经元丢失是许多神经退行性疾病(如脑卒中,老年性痴呆症,帕金森症,肌萎缩性脊髓侧索硬化症和亨廷顿舞蹈症等)的共同原因。因此,揭示神经元死亡机制是防治神经退行性疾病关键所在。徐天乐研究组长期致力于研究神经退行性疾病过程中,神经元死亡的离子通道机制。在先期研究中(Gao et al. Neuron, 2005; Duan et al. Journal of Neuroscience, 2011; Zeng et al. Journal of Neuroscience, 2013),研究人员重点关注了神经元质膜ASIC1a通道的作用。经过两年多的潜心研究,王宜之及其合作者发现,除了质膜之外,神经元内部的线粒体内膜上也表达有功能性ASIC1a(mtASIC1a)。进一步研究发现mtASIC1a调控了一种决定神经元存活或死亡的重要机制 -线粒体膜通透性转换(mitochondrial permeability transition pore, MPTP)。在ASIC1a基因敲除小鼠的线粒体中,钙离子容量(calcium retention capacity)和钙离子摄取速率显著增高,提示MPTP活动受到抑制。与此同时,ASIC1a基因敲除对经由线粒体的活性氧自由基(reactive oxygen species, ROS)诱导的神经元死亡具有明显保护作用。此外, ASIC1a基因敲除还影响线粒体的形态以及部分线粒体关键蛋白的表达和基础ROS水平。综上所述,该研究在揭示出线粒体ASIC1a的基础上,阐明了其在神经元死亡信号通路中的重要作用,为研究神经退行性疾病的机理和优化疾病防治对策提供了新思路,具有重要的理论意义和应用价值。
研究工作得到美国得克萨斯大学休斯顿健康科学中心朱曦教授和加拿大Dalhousie大学董先平教授大力支持,并获得了国家自然科学基金重点项目,国家自然科学基金重大研究计划集成项目和中国博士后基金等项目的资助。
全文连接:http://www.ncbi.nlm.nih.gov/pubmed/23852371
