近日,国际学术期刊《Stem Cells》在线发表了上海交通大学基础医学院/上海市免疫学研究所王宏林课题组题为“Autocrine
Interleukin-6 Drives Skin-Derived Mesenchymal Stem Cell Trafficking
via Regulating Voltage-Gated Ca2+
Channels”的研究论文,报道了自分泌的IL-6在MSCs(Mesenchymal Stem Cells,
MSCs)迁移过程中的重要作用。
MSCs作为干细胞的一种,因其具有多向分化潜能,在损伤组织修复中发挥重要作用,并在再生医学领域中具有广泛的应用前景。除骨髓MSCs外,皮肤中也存在有MSCs,皮肤是人体最大的器官,能够提供大量的MSCs。在炎症因子的刺激下,MSCs能够高分泌IL-6,这些IL-6能够抑制T细胞的增殖以及树突状细胞的分化和功能,同时IL-6也能够促进MSCs的增殖,抑制MSCs的凋亡和维持MSCs的干性,但IL-6在MSCs迁移过程中的作用并不清楚。然而,MSCs在临床治疗中的应用则要求细胞能够高效的迁移到靶组织部位。因此,研究IL-6对MSCs迁移的调控机制具有重要生理意义。
博士后柯芳等发现,从小鼠皮肤中分离得到的MSCs在炎症环境下能够分泌产生大量IL-6,结合IL-6
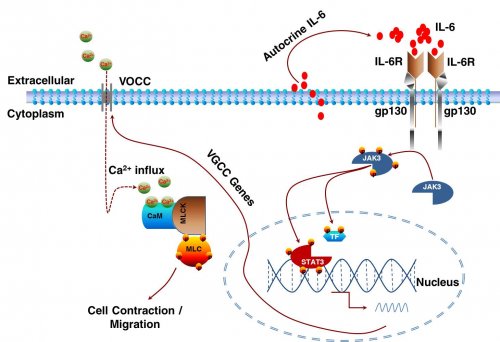
基因剔除小鼠的皮肤MSCs在体内外的免疫抑制作用证实皮肤MSCs在体内的免疫抑制功能需要IL-6信号通路的参与,利用细胞实时粘附监测技术、transwell实验技术以及活体成像技术证明自分泌的IL-6可调节皮肤MSCs的迁移。课题组进一步通过钙成像技术和膜片钳技术证实IL-6信号通路是通过调控电压门控的钙离子通道来调节皮肤MSCs的迁移的。至此,该研究首次揭示了IL-6信号通路调节的电压门控钙离子通道在MSCs迁移中的重要作用,揭示了MSCs向炎症部位迁移以及其体内免疫抑制功能的新机制。
