
近日,上海交通大学医学院-国家热带病研究中心全球健康学院殷堃课题组在国际期刊Chemical Engineering Journal在线发表了题为“Spatiotemporal dual-dimensional separation enables ultra-simple one-pot CRISPR-based molecular diagnostics”的研究论文。该研究构建了一种基于时空双维度分隔的一步法RPA-CRISPR病原体快速检测平台,通过设计物理屏障装置,实现两分隔体系自发动态融合,解决气溶胶污染及体系不兼容问题,实现简便、灵敏、特异的病原体检测,为开发理想病原体检测方法提供技术支撑。
近年来,基于CRISPR/Cas系统的检测方法已成为分子诊断技术开发重点。与等温扩增方法如RPA联用可提升基于CRISPR检测的灵敏度,然而,分步法操作涉及扩增产物开盖转移步骤,增加气溶胶污染的风险。因此,将RPA与CRISPR反应整合到一管式封闭体系中可避免此问题,但一管式检测面临两体系不兼容问题,检测效率显著下降。为应对这一挑战,已有研究建立时间或空间维度分隔的方法,先物理分隔或通过光降解引物分隔两体系,后通过离心或光照操作使RPA与CRISPR反应混合,实现灵敏的一管式RPA-CRISPR检测。然而,这些方法依赖中间操作实现分步反应,因此,一种简便、自发进行的一管式检测平台仍然亟待开发。
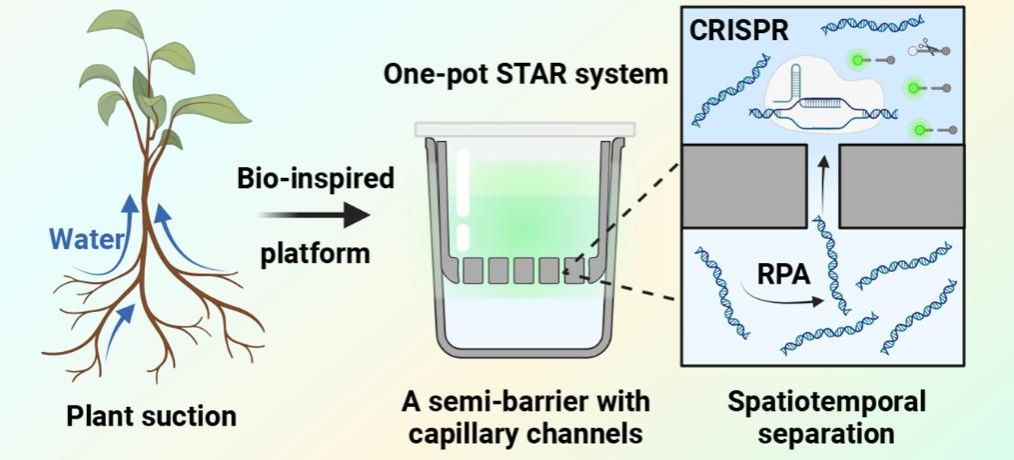
为解决体系不兼容问题,本研究首先设计了一种“管中管”结构,通过3D打印技术设计并打印底部包含数个毛细通道的内管作为物理半屏障装置,实现时空双维度分隔并能自发进行的RPA-CRISPR一管式反应。内管底部作为物理屏障在空间维度分隔两体系,同时,内管底部垂直贯穿的数个毛细通道将两体系连接起来,随着下方RPA反应进行,浓度逐渐增高的核酸扩增产物经由毛细通道向上扩散至上方CRISPR体系中,与crRNA互补配对结合,激活Cas12a蛋白对荧光报告探针的反式切割活性,并产生荧光信号,以此形成时间维度分隔。这种基于时空双维度分隔的一步法CRISPR/Cas检测方法无需任何中间操作,反应开始后两体系可逐渐自发动态融合,实现真正简便的一步法检测。该平台被用于沙门氏菌检测,表现出良好特异性及灵敏度,为开发理想病原体检测方法提供技术支撑。
上海交通大学医学院-国家热带病研究中心全球健康学院硕士研究生李慧敏为本文的第一作者,胡沁沁副研究员和殷堃研究员为本文的共同通讯作者。本研究得到国家自然科学基金项目、上海市自然科学基金项目、海南省重点研发项目等基金支持。
