近年来,mRNA作为生物医药领域的变革性技术,不仅在新冠疫苗研发中实现了成功落地,也在肿瘤免疫治疗、蛋白替代治疗、基因编辑等方向展现出广阔前景。然而,当前主流mRNA递送载体普遍存在“天然嗜肝性”,难以实现肝外器官的精准递送,已成为制约mRNA疗法进一步拓展的重要瓶颈。天然包膜病毒及病毒样颗粒在肝外靶向mRNA递送方面显示出巨大潜力,但其免疫原性较高、制备工艺复杂、靶向可编程性不足以及潜在生物安全风险等问题,显著限制了临床转化与规模化应用。
2026年4月,基础医学院高小玲教授课题组联合徐颖洁团队与樊晨团队在《ACS Nano》发表题为“Self-Assembling Enveloped Virus-Mimicking Particle for Extrahepatic Targeting mRNA Delivery”的研究论文。该研究借鉴包膜病毒的天然自组装与RNA转运模式,提出包膜病毒模拟颗粒(Enveloped Virus-Mimicking Particle, EVMP)的从头设计策略,构建出兼具安全性、高效性与肝外靶向能力的非病毒mRNA递送平台。EVMP的设计为仿生mRNA递送载体的后续开发及肝外mRNA疗法的临床拓展提供了新的思路。
研究团队跳出传统病毒载体“直接改造”的范式,转而采用“功能模拟、从头设计”的策略构建EVMP。首先,借鉴包膜病毒的组装机制,通过分子动力学模拟解析代表性包膜病毒结构蛋白——Gag蛋白膜定位区与RNA结合区的动态作用模式及关键结构域。在此基础上,团队以模块化思路设计了12种代表性的病毒模拟肽(Virus-Mimicking Peptide, VMP)范式,将Gag蛋白的膜定位模块与 RNA 结合模块整合于同一短肽中,结合虚拟筛选、定向进化及N端脂肪酸修饰优化策略提升VMP的mRNA递送潜力,最终筛选获得综合性能最优的病毒模拟肽。其次,研究摒弃易诱发免疫反应的病毒包膜蛋白,转而利用磷脂包膜在颗粒组装与体内器官趋向性中的关键作用,构建覆盖中性磷脂、阴离子磷脂及辅助磷脂的天然磷脂库;通过对磷脂种类与比例进行精细调控,赋予EVMP高效的体内外mRNA递送能力和灵活可调的肝外器官靶向特性(图 1)。
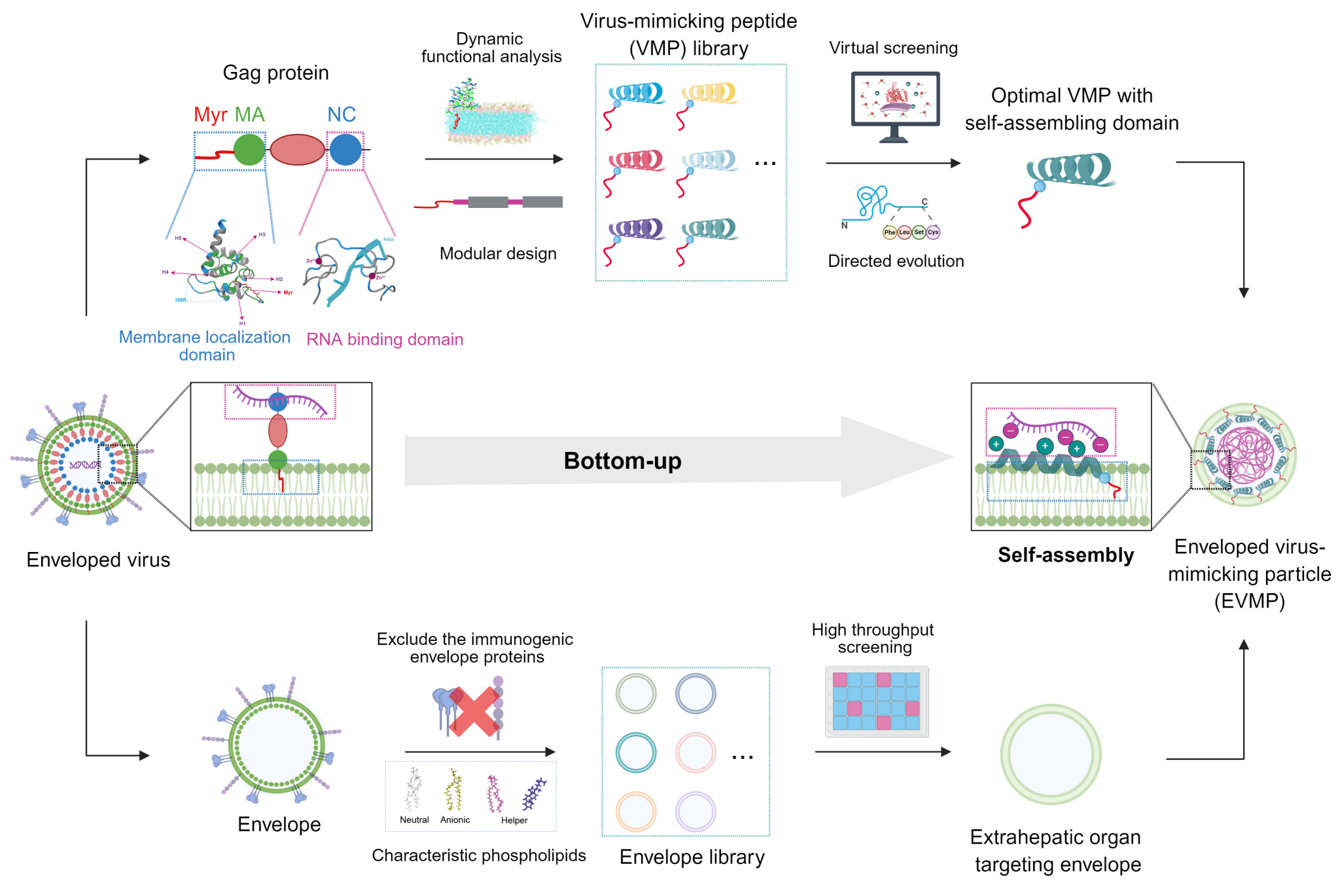
图1 包膜病毒模拟颗粒(EVMP)自下而上的构建策略
在制备工艺上,VMP、磷脂与mRNA可通过一步法自组装形成EVMP,流程简洁且具备放大潜力,避免了传统病毒样颗粒制备过程中步骤繁琐、成本高昂的缺点。体内研究显示,EVMP具有天然的肝外靶向倾向,能够在肺、脾等肝外器官实现选择性表达。其中,肺靶向EVMP的转染效率显著优于金标准MC3/DOTAP LNP(图 2)。在转移性肺部肿瘤模型中,EVMP递送IL-12 mRNA可介导高效肿瘤免疫治疗,通过重塑肿瘤免疫微环境显著减少肺部转移瘤结节数量并延长荷瘤小鼠生存期。
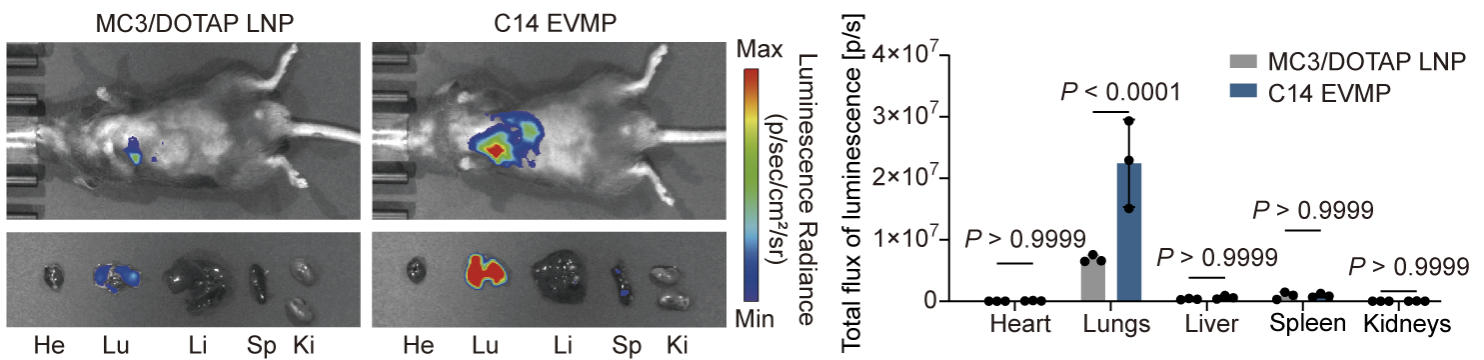
图2 肺靶向EVMP在肺部的转染效率显著高于MC3/DOTAP LNP
安全性方面,EVMP长期给药耐受性良好,未见明显脏器毒性、肝肾功能损伤或急性炎症反应;同时其免疫原性较低,重复给药条件下体内递送效能保持稳定,不诱导全身性记忆免疫应答增强或中和抗体升高,从而在一定程度上突破了传统包膜病毒载体在安全性与重复给药上的核心限制。
综上,该研究验证了“包膜病毒功能模拟”的路径可行性,通过VMP和包膜磷脂的协同设计与自组装,构建了兼具安全性、高效率与肝外靶向可调性的非病毒mRNA递送系统。作为一种全新的非病毒递送平台,EVMP展现出良好的临床转化潜力,有望为下一代兼顾递送效率、安全性与规模化生产的非病毒载体研发,以及肝外器官靶向基因治疗的临床推进提供关键理论依据与技术支撑。
基础医学院高小玲课题组博士研究生余人和与助理研究员黄宇坤为该论文共同第一作者。高小玲教授、徐颖洁研究员、樊晨研究员及黄宇坤助理研究员为共同通讯作者。本研究获得国家重点研发计划和国家自然科学基金等项目资助。