2020年3月17日,上海交通大学医学院基础医学院黄菊研究员课题组和李乾研究员课题组合作Cell Reports在线发表了文章“Chromatin-binding protein PHF6 regulates activity-dependent transcriptional networks to promote hunger response” 。该研究发现Borjeson-Forssman-Lehmann (BFL)综合症蛋白plant homeodomain finger protein 6 (PHF6),一种重要的染色质结合蛋白,在下丘脑弓状核AgRP神经元中作为转录抑制子,调控及早基因(immediate early genes, IEGs)的表达,进而影响小鼠饥饿驱动的摄食行为。
饥饿驱动的摄食行为主要由下丘脑弓状核AgRP神经元所调控,这些神经元可以感知机体的能量状态,并决定动物体是否去觅食。已有研究表明饥饿能够诱导AgRP神经元中转录谱的显著变化,但是人们至今不清楚上游转录因子或表观遗传调控因子(如组蛋白乙酰转移酶,甲基转移酶,染色质重塑酶等)对于AgRP神经元不同营养状态下饥饿反应基因的调控方式。黄菊和李乾团队经过深入研究发现AgRP神经元中特异高表达PHF6,且PHF6的表达会受到机体营养状态调控。通过神经元类型特异性的RNA-seq与ChIP-seq,研究人员发现缺失了PHF6会使AgRP神经元的转录谱向饥饿状态转变,尤其及早基因IEGs的表达水平显著上调,因此损害了饥饿状态下IEGs快速而充分的诱导。这是由于正常情况下PHF6结合在IEGs的启动子区域,并发挥转录抑制的作用。在功能上,PHF6对神经元活动依赖的IEGs的转录抑制作用会影响摄食行为,PHF6条件性敲除小鼠不仅表现出下降的饥饿激发的食欲,而且可以帮助小鼠抵抗反复地节食/复食引起的体重增加。
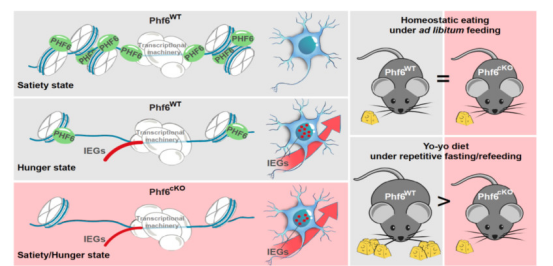
PHF6作为BFL综合症的致病蛋白,在神经系统中的功能十分重要,先前的研究主要探索了它在大脑皮层发育和认知功能中的作用。本研究则聚焦于PHF6在成年动物下丘脑神经元和本能行为中的功能,发现PHF6作为一种神经元亚群特异的转录阻遏因子,通过调节不同营养状态下的转录谱进而调控动物的摄食行为,为我们理解染色质结合蛋白如何调控动物的适应性行为提供了一个崭新的视角。
本研究由上海交通大学医学院黄菊课题组和李乾课题组合作完成,上海交通大学医学院博士研究生干林华和工作人员孙静静为论文共同第一作者,黄菊研究员和李乾研究员为共同通讯作者。
原文链接:https://doi.org/10.1016/j.celrep.2020.02.085