2022年5月23日,上海交通大学基础医学院生化与分子细胞生物学系童雪梅教授课题组、上海市免疫学研究所李斌研究员课题组和复旦大学附属华山医院/脑科学与转化研究院杨辉研究员等合作在Nature Metabolism杂志在线发表题为Non-oxidative pentose phosphate pathway controls regulatory T cell function by integrating metabolism and epigenetics的研究论文,揭示非氧化磷酸戊糖途径(非氧化PPP)调控调节性T细胞(Treg)功能的新作用及其机制。伦敦帝国理工学院Margarita Dominguez-Villar博士在同期Nature Metabolism杂志为该研究撰写News & Views特评,认为该文章发现非氧化PPP在Treg活化和功能调控中的中心地位(a central regulator)。

表达特征转录因子Foxp3的Treg是一类具有免疫抑制功能的CD4+ T细胞亚群,维持机体免疫系统稳态,防止免疫过激诱发自身免疫病。非氧化PPP包括4个代谢酶催化的5步可逆反应,可以通过改变代谢物流向来满足细胞的功能需求。非氧化PPP是否参与Treg功能调控尚不清楚。
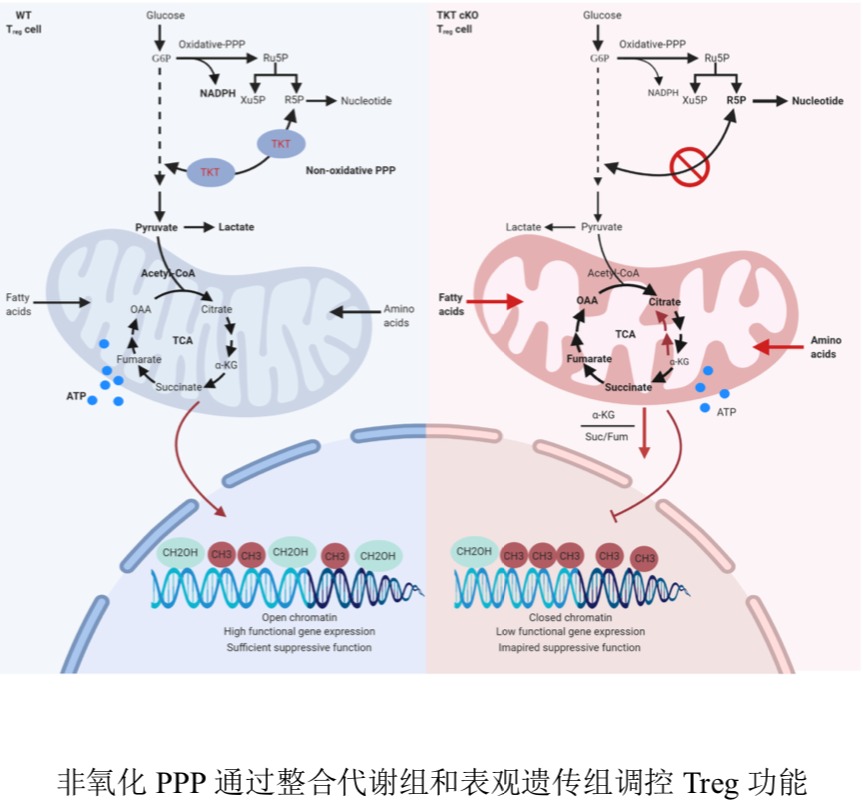
转酮醇酶TKT是非氧化PPP中催化两步可逆反应的代谢酶。童雪梅团队已发现TKT在肝脏、脂肪和肠道中调控糖脂代谢平衡的重要作用(Li M et al, Cancer Research, 2019; Tian N et al, Diabetes, 2020; Tian N et al, Cell Death & Disease, 2021)。在本研究中,Treg特异性敲除TKT的小鼠出生3周后发生严重自身免疫性疾病,并且在断奶之后相继死亡,其表型与缺失Foxp3基因的小鼠相似。进一步研究发现,敲除TKT在不改变Treg数目和转录因子Foxp3 水平的情况下,抑制Treg的免疫抑制功能。其机制是,TKT缺失导致Treg的NADPH 减少和氧化应激增加,葡萄糖进入线粒体氧化减少,脂肪酸氧化增加,氨基酸分解代谢显著增强,分解代谢重构使线粒体功能受损。同时,被氧化应激和线粒体损伤诱发的还原性TCA循环使α-酮戊二酸/琥珀酸及α-酮戊二酸/富马酸比率降低,DNA甲基化增加,抑制Treg特征性功能基因表达,导致其免疫抑制性功能丧失。
文章发现非氧化PPP中的转醛醇酶(TAL)对维持效应性Treg特征性功能基因表达也不可或缺。此外,在自身免疫性病人外周血 Treg细胞中,TKT水平显著降低。
此研究首次揭示非氧化PPP整合三大营养物质代谢和表观遗传修饰从而控制Treg功能,将为通过调控Treg功能防治自身免疫性疾病和其他免疫相关疾病提供新思路。
上海交通大学医学院博士生刘琪、阿拉巴马大学伯明翰分校博士生朱方明和上海市免疫学研究所博士生刘鑫男是该研究论文的共同第一作者。此项研究得到复旦大学医学院叶丹研究员、海军军医大学附属长征医院风湿免疫科徐沪济主任、上海交通大学附属仁济医院沈南主任、上海交通大学基础医学院徐天乐教授、清华大学药学院胡泽平研究员、阿拉巴马大学伯明翰分校胡晖教授等合作实验室的大力协助。通讯作者为童雪梅教授、李斌研究员和杨辉研究员。该研究获国家重点研发计划、国家自然科学基金委和上海市科学技术委员会科学基金委等资助。
相关论文和特评信息:https://www.nature.com/articles/s42255-022-00575-z,
https://www.nature.com/articles/s42255-022-00574-0