随着我国经济快速发展和人民生活水平的提高,大众的生活方式也发生着深刻变迁。现如今,脂肪肝、高脂血症等脂代谢紊乱疾病的患病率持续攀升。脂代谢紊乱如同无声的“血管腐蚀剂”,容易引起血管炎症与损伤,促进动脉粥样硬化、主动脉瘤等大血管病变,成为导致患者不良结局甚至死亡的主要原因之一。因此,深入揭示脂代谢紊乱致血管病变的分子机制,寻找潜在有效的干预策略,对于降低心血管事件风险以及死亡率具有重要的临床意义和紧迫的现实需求。
2026年2月27日,附属六人民医院陆炎课题组与上海交通大学/复旦大学阮承超课题组在Nature Immunology期刊合作发表题为“Sparcl1 mitigates abdominal aorticaneurysm through inhibiting lymphangiogenesis-mediated TLS formation”的研究论文。

该研究发现血管组织驻留巨噬细胞(Vascular tissue-resident macrophages,VRMs)分泌的基质蛋白Sparcl1通过阻断病理性淋巴管新生,抑制血管外膜三级淋巴样结构形成,从而改善血管炎症损伤与动脉瘤病变(见示意图)。
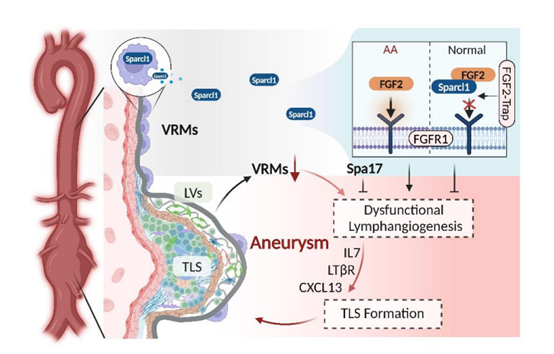
示意图:本研究工作模型
研究人员首先分析了主动脉瘤临床样本和小鼠模型的单细胞转录组数据集,发现血管外膜Lyve1+原位巨噬细胞数量显著减少。随后,在高脂血症模型(低密度脂蛋白受体LDLR基因敲除小鼠)的基础上,构建了清除Lyve1+巨噬细胞的双敲小鼠(Lyve1-Cre; Csf1rflox/flox; LdlrKO),证实血管外膜Lyve1+巨噬细胞抑制主动脉瘤进展,缓解血管炎症与损伤。研究人员进一步运用多组学筛选和分析,发现血管外膜Lyve1+巨噬细胞表达和分泌的基质蛋白Sparcl1表达显著降低。功能和机制研究证实,Sparcl1通过与成纤维生长因子FGF2结合,阻断其下游NF-kB通路的激活,从而抑制炎症因子和趋化因子的表达,改善血管炎症损伤和主动脉瘤进展。为了验证Sparcl1蛋白的治疗潜力,研究人员开发了功能性多肽Spa17,并通过多种模型证实其具有改善主动脉瘤和血管炎症损伤,以及抑制淋巴管生成、免疫细胞浸润的作用,表明Sparcl1蛋白具有显著的治疗潜力。综上所述,这一研究成果为理解脂代谢紊乱致血管病变提供了新视角,进一步揭示了高脂血症相关血管炎症损伤和腹主动脉瘤发生发展的分子机制,并通过设计以Sparcl1蛋白为基础的功能性多肽,为开展临床转化和应用研究提供了坚实的科学依据。
附属第六人民医院陈梅华博士后是本文的第一作者,复旦大学基础医学院滑艺杰博士为共同第一作者。附属胸科医院阮承超研究员、复旦大学基础医学院庄涛副研究员、附属第六人民医院陆炎研究员、复旦大学附属中山医院董智慧教授和附属瑞金医院卢湾分院李燕医师为本文共同通讯作者。该工作得到了国家自然科学基金、科技部重点研发计划和四大慢病重大专项等项目资助。
