近日,上海交通大学医学院钟清、付婉团队在Advanced Science发表研究成果,首次揭示线粒体在铁死亡中的全新信号转导机制:线粒体渗透性转换孔(mPTP)开放后释放氧化损伤的线粒体DNA(ox-mtDNA),激活cGAS–STING通路并诱导“铁自噬”,从而放大铁死亡反应。该发现不仅回答了“铁死亡中线粒体为何肿胀、肿胀后发生什么”的关键问题,也为肿瘤治疗提供了新的联合用药策略。

铁死亡是一种由铁依赖性脂质过氧化驱动的程序性细胞死亡方式,与癌症、神经退行性疾病等密切相关。尽管线粒体肿胀是铁死亡的典型形态学特征,但其机制和功能长期未明。研究团队发现,在Erastin、RSL3等铁死亡诱导剂作用下,线粒体出现明显肿胀并伴随mPTP开放。应用mPTP抑制剂环孢素A(CsA)或通过基因编辑敲除其关键组分CypD,均可显著抑制脂质过氧化和细胞死亡,表明mPTP开放是铁死亡发生的必要步骤。
进一步机制研究显示,mPTP开放会将氧化损伤的mtDNA释放至胞质。超分辨成像证实,铁死亡过程中mtDNA从线粒体转移至胞质区域。与此同时,抑制mtDNA修复酶FEN1或OGG1可增加氧化mtDNA的积累,并显著增强细胞对铁死亡诱导剂的敏感性;这一效应依赖mPTP及相关通道蛋白ANT等组分。
释放至胞质的ox-mtDNA被DNA感知通路cGAS识别,进而激活STING–TBK1信号轴。抑制cGAS或STING可有效阻断铁死亡及OGG1抑制带来的增强效应。研究表明,cGAS–STING的激活促进铁蛋白通过自噬途径降解,即“铁自噬”,增加细胞内不稳定铁池(LIP),进而通过芬顿反应放大脂质过氧化,形成正反馈环路,加速铁死亡进程。
基于上述机制,研究团队在NCI-H1299肺癌细胞移植瘤模型中开展体内实验。结果显示,铁死亡诱导剂IKE与OGG1抑制剂TH5487联合用药,相较单药治疗更显著抑制肿瘤生长,且未观察到明显毒性。肿瘤组织中ACSL4上调、GPX4下降,提示铁死亡在体内被有效激活。
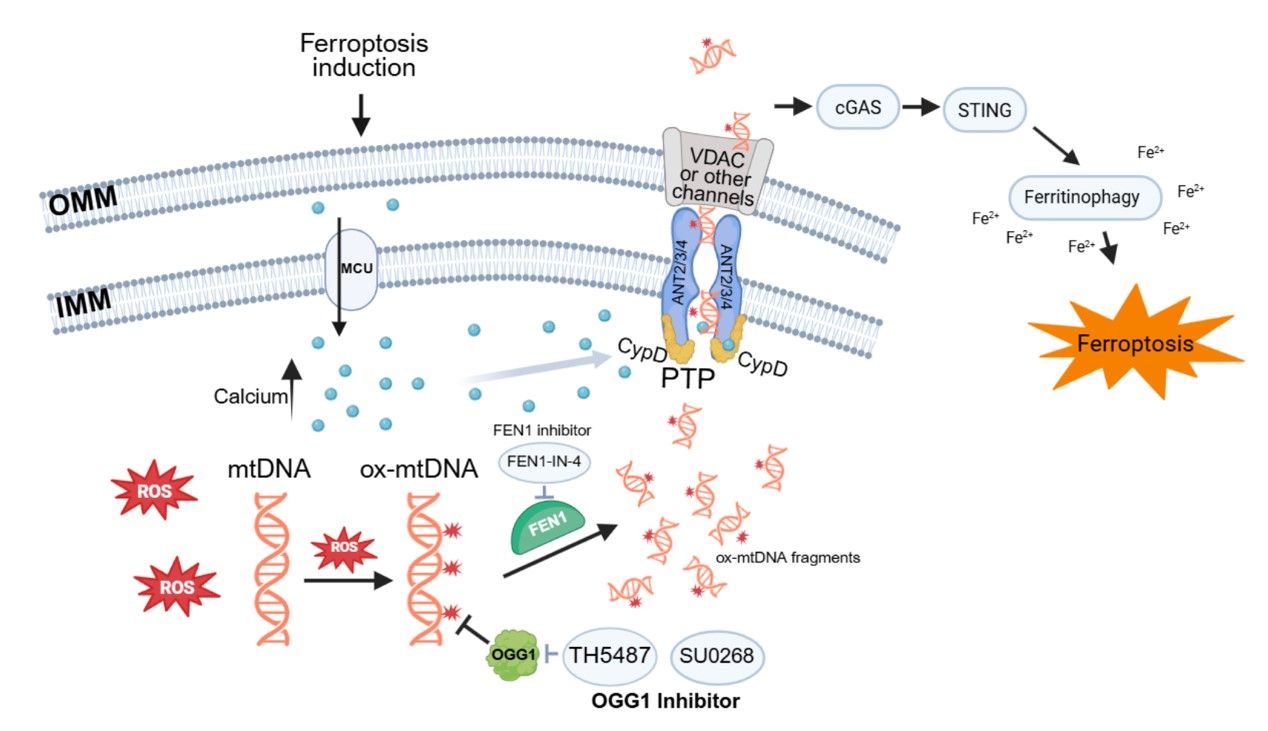
该研究首次系统提出“mPTP–mtDNA–cGAS–STING”铁死亡信号轴,拓展了人们对铁死亡调控网络的认识。研究将线粒体功能失衡、DNA损伤修复、天然免疫信号与铁代谢紧密联系起来,揭示了铁死亡的信号放大机制,也为“抑制mtDNA修复+诱导铁死亡”的联合抗癌策略提供了有力的临床前证据。
上海交通大学医学院周红博士,助理研究员付婉为本文的共同第一作者,上海交通大学医学院研究员钟清、助理研究员付婉为本文的共同通讯作者。本研究还得到了上海交通大学医学院公共平台的技术支持。
