大脑作为生物钟的执行者,以24小时为周期调控睡眠、进食等多种重要生理活动。自然状态下,生物体倾向于在活动期进食,在休息期减少摄入。对人类而言,这意味着白天是主要的进食窗口;而对夜行性小鼠来说,夜晚才是它们的“饭点”。 然而,现代生活方式——如熬夜工作、跨时区旅行、深夜使用电子设备——常常打乱这种自然节律,进而诱发肥胖、2型糖尿病等代谢相关疾病。
长期以来,下丘脑被认为是控制进食昼夜节律的核心脑区。2026年2月19日,上海交通大学医学院徐天乐教授团队与美国北卡罗来纳大学教堂山分校(UNC)宋娟教授团队合作在Neuron在线发表题为Ventral hippocampal NPY neurons regulate circadian feeding in mice的研究论文。
在这项研究中,作者发现腹侧海马,一个与情感记忆密切相关的脑区,在进食节律调控中也扮演了意想不到的关键作用。研究人员聚焦于腹侧海马的一类表达神经肽Y(neuropeptide Y, NPY)的抑制性中间神经元(NPY-INs)。通过监测小鼠在正常节律下以及节律紊乱下的NPY-INs活性,发现正常节律下:白天(小鼠休息期),NPY-INs活性较低,进食量少;夜晚(小鼠活动期),NPY-INs活性增强,进食量增加。如果让小鼠长期处于夜晚开灯(light at night)或白天黑暗(dark at day)的环境,NPY-INs的节律性活动会消失,进食节律也随之打乱——该吃的时候不吃,不该吃的时候反而多吃。更有趣的是,腹侧海马NPY-INs会随着昼夜交替切换信号传递方式:白天主要释放NPY,抑制进食。夜晚则主要释放GABA(一种抑制性神经递质),促进进食。这就像同一个开关,在不同时间通过不同线路控制同一盏灯。
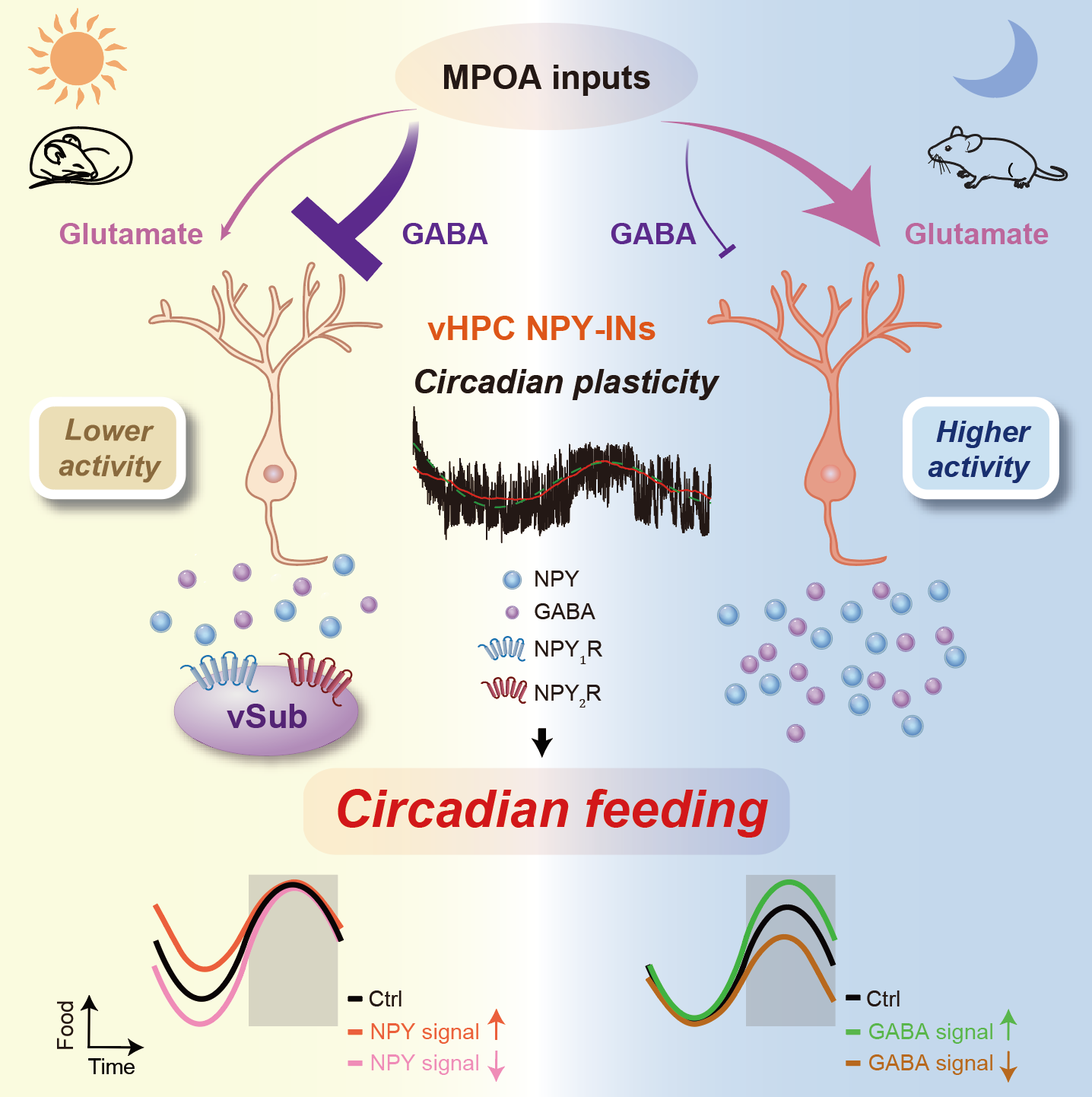
图1.腹侧海马NPY-INs调控小鼠进食昼夜节律
那么,NPY-INs是如何感知昼夜的时间差呢?通过病毒逆向示踪实验,研究人员发现,NPY-INs接收来自内侧视前区(media preoptic area, MPOA)神经信号输入——这是一个已知接收来自主生物钟视交叉上核(suprachiasmatic nucleus, SCN)输入的区域。MPOA神经元通过单突触释放兴奋性谷氨酸和抑制性GABA信号,协同调节NPY-INs的神经活性,形成“白天抑制、夜晚兴奋”的节律模式。最终,这些信号被传递到海马的下游区域——腹侧下托(ventralsubiculum, vSub),通过NPY受体抑制该区域活动,从而控制进食行为。这一“MPOA → NPY-INs → vSub”的神经环路(图1),跳出了传统“下丘脑中心论”的认知,首次揭示了下丘脑生物钟系统如何与海马进食调控网络相连接。
上海交通大学医学院博士研究生焦志涵和边鑫以及博士后吴延娇为论文的共同第一作者。上海交通大学医学院宋兴磊博士和徐天乐教授、美国UNC宋娟教授为论文的共同通讯作者。上海交通大学医学院松江研究院李亚东研究员提供了合作支持。该研究得到了国家自然科学基金委、科技创新2030-脑科学与类脑研究重大项目、上海市教委高水平地方高校建设创新团队项目等项目的支持。
