
2024年3月4日,Nature子刊《Bone Research》杂志(中科院一区, IF 12.7)在线发表了上海交通大学医学院附属新华医院骨科张晓玲教授与中国科学院上海营养与健康研究所吕伟教授和华东师范大学纳米医学与生物材料研究室程义云教授的合作论著,题目为“Targeted knockdown of PGAM5 in synovial macrophages efficiently alleviates osteoarthritis”。张晓玲教授的直博生刘宇航为该论文的第一作者。研究团队发现了调控巨噬细胞极化的关键分子——磷酸甘油酸变位酶家族成员5(PGAM5),在骨关节炎(OA)的发生发展中起重要作用,靶向敲除滑膜巨噬细胞PGAM5可以有效治疗OA。
OA是最常见的衰老退变性的关节疾病,全世界约2亿人受到OA的影响,随着人口老龄化的加剧,其患病率呈逐年增加趋势,OA病变累及整个关节,包括软骨、滑膜、及软骨下骨等,致残率高居全球第二位,给家庭及社会带来较大的经济负担和压力。目前临床对于OA主要是症状产生后的对症治疗,使用镇痛药物等保守治疗缓解症状,直至晚期关节置换,尚缺乏早期防治手段。探究OA早期关节免疫细胞的功能变化并靶向调控有望使OA治疗关口前移。
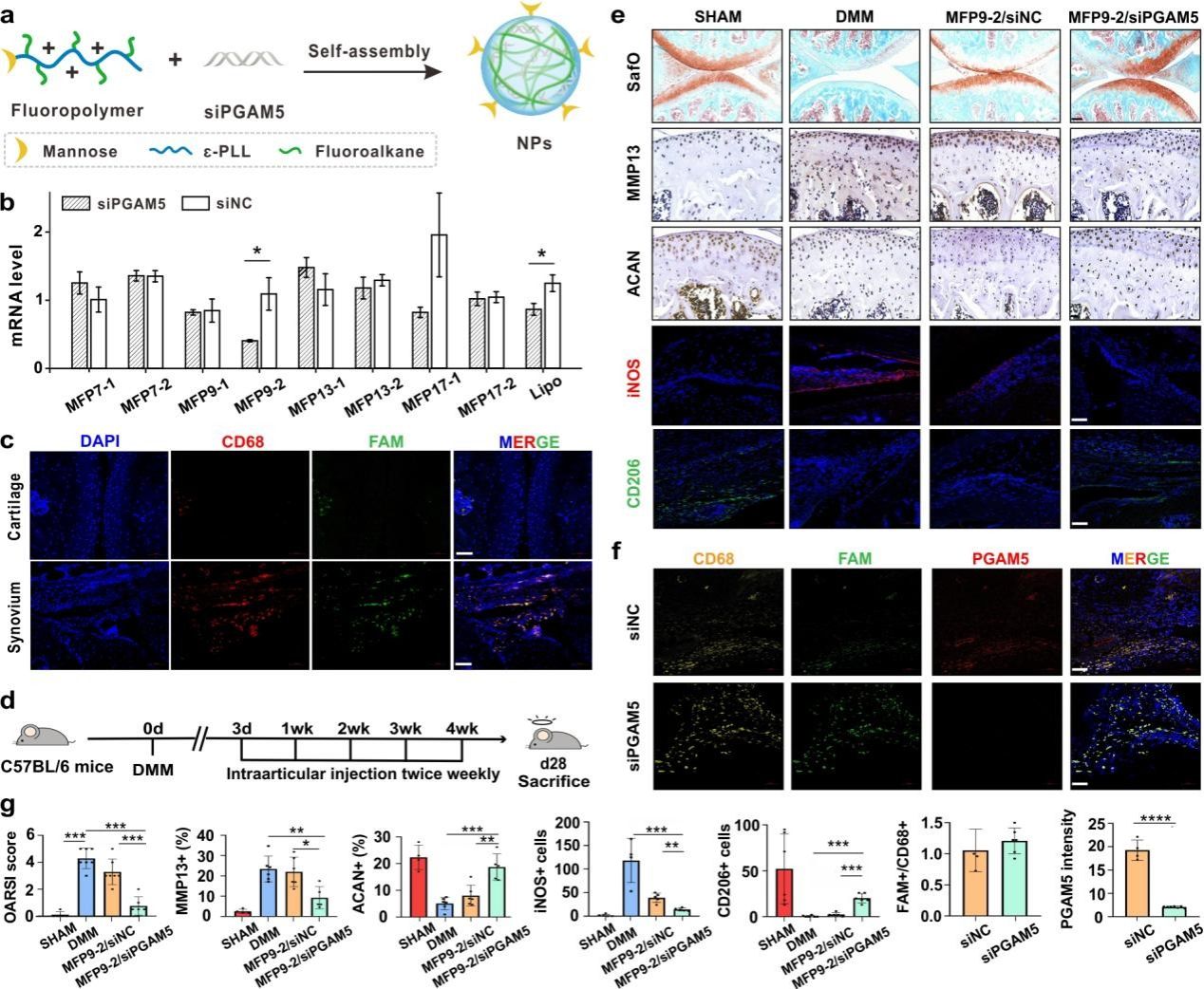
张晓玲教授团队通过单细胞组学分析及临床OA病人滑膜标本,发现OA滑膜巨噬细胞的PGAM5水平显著提高。为了验证PGAM5在滑膜巨噬细胞中的作用,研究团队构建了PGAM5 flox-Lyz2 Cre的条件性敲基因小鼠,该小鼠在巨噬细胞中特异性缺失PGAM5。利用RNA测序技术等大量体内外实验,发现PGAM5可以调控巨噬细胞M2向M1的复极化,分泌大量炎症因子,从而促进软骨基质的降解及OA的发生发展。进一步团队构建了PGAM5 flox, β-catenin flox-Lyz2 Cre的条件性敲基因小鼠,揭示了PGAM5通过与Dvl2蛋白结合抑制β-catenin信号,进而影响巨噬细胞极化。为实现稳定的在体巨噬细胞靶向高效递送,团队利用甘露糖修饰含氟聚合物,搭载PGAM5的siRNA,通过关节内注射的方式,有效靶向抑制小鼠滑膜巨噬细胞PGAM5的表达,缓解OA症状。
研究团队首次揭示了PGAM5在滑膜巨噬细胞极化中的关键作用及机制,提供了全新的OA精准靶向免疫治疗策略,为临床早期干预OA提供理论依据。该研究得到国家自然科学基金委、科技部和上海市科委等经费的支持。
