囊性纤维化是一种常染色体隐性遗传疾病。其根本原因是位于第7号染色体上的CFTR基因发生突变。CFTR蛋白是细胞膜上一种负责氯离子转运的通道蛋白。CFTR功能障碍导致氯离子和水分跨膜转运异常,进而引起全身外分泌腺分泌的黏液异常粘稠、淤积。囊性纤维化一种致命的疾病。在高加索人中较为常见,随着诊断意识提高和基因检测普及,中国报道的病例逐渐增多。全球已发现超过2000种CFTR基因突变类型。其中最常见的F508del突变会导致CFTR通道蛋白折叠异常、运输受阻,无法在细胞膜上形成功能性的氯离子通道,进而引发呼吸道、消化道等多器官功能障碍。当前临床上主要采用校正剂(如Lumacaftor、Tezacaftor、Elexacaftor)联合增效剂(如Ivacaftor)进行治疗,但部分患者仍存在疗效不佳或对药物不敏感的问题。

近日,上海交通大学医学院附属松江医院/松江研究院蔡时青研究团队在《Molecular Therapy》期刊发表题为“PKC activators improve the function of biogenesis-deficient CFTR channels”的研究论文,揭示了一类新型小分子化合物——蛋白激酶C(PKC)激动剂,可通过全新机制提升突变CFTR通道蛋白的生物生成效率,并与现有药物形成叠加效果,为囊性纤维化患者提供了新的治疗策略。
研究发现,PKC激动剂IDB和DOPPA能够从源头上增强CFTR蛋白的合成。与现有药物主要协助蛋白折叠或运输的机制不同,PKC激动剂通过激活PKCε信号通路,在蛋白翻译阶段对新生CFTR肽链进行磷酸化修饰,避免其因折叠缺陷被过早降解。这一修饰过程不仅能稳定CFTR mRNA,还可持续提升功能性CFTR蛋白的表达量(图)。形象地说,若将现有校正剂比作“修理工”,PKC激动剂则更像“生产加速器”,它们通过增加可供校正的CFTR蛋白,从而与现有药物产生协同增效作用。
在F508del纯合突变小鼠模型中,IDB能显著提高肺部成熟CFTR蛋白的表达与膜定位。同时,IDB处理也有效缓解了铜绿假单胞菌感染引起的小鼠体重下降及肺部炎症,与现有药物联用后效果进一步增强。尤为重要的是,对于现有药物无效的部分突变体(如Q98R、N1303K等),IDB单独使用即可恢复CFTR突变通道功能,显示出其潜在的应用前景。
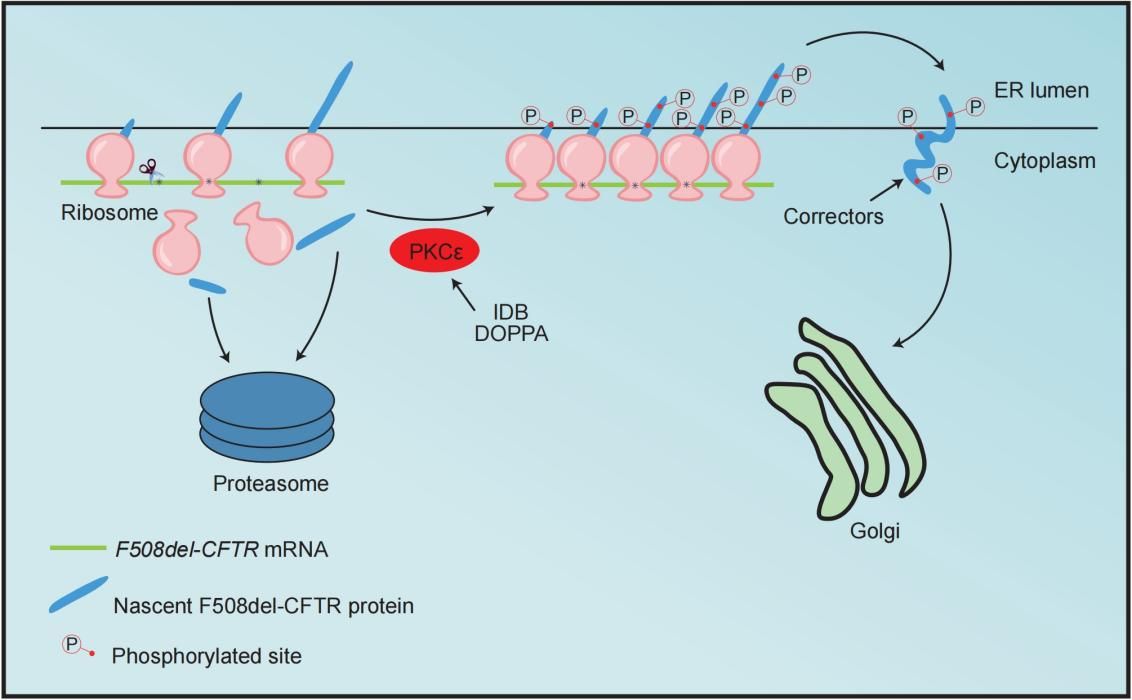
图 PKC激动剂通过磷酸化作用提高CFTR突变体的表达量
总的来说,该研究不仅揭示了一条此前未被重视的CFTR生物生成调控通路,也为开发针对多种CFTR突变类型的“放大器”类药物提供了理论依据。目前,研究团队正进一步探究其他激酶对CFTR生物生成的影响,同时优化PKC激动剂的结构和功能,并探索其在其他离子通道病中的应用潜力。
上海交通大学医学院附属松江医院/松江研究院蔡时青研究员和复旦大学附属中山医院沈雳教授为该论文的共同通讯作者,上海理工大学博士后叶士伟和上海交通大学医学院附属松江医院/松江研究院刘喜娟为该论文的共同第一作者,中国科学院脑科学与智能技术卓越创新中心的康心蕾也做出了重要贡献。研究获国家自然科学基金委员会和科学技术部项目支持。
