近日,由公共卫生学院栾洋团队发表于毒理学领域权威期刊Archives of Toxicology的研究,首次结合纠错NGS技术(error-corrected Next-Generation Sequencing, ecNGS)与DNA甲基化定量分析,系统评估了N-亚硝基二甲胺(NDMA)在小鼠体内的遗传毒性与突变特征,并基于实验数据推算出其突变诱导的每日允许暴露量(PDE)。全文链接Arch Toxicol. 2025 Nov;99(11):4665-4676. doi: 10.1007/s00204-025-04166-1.。
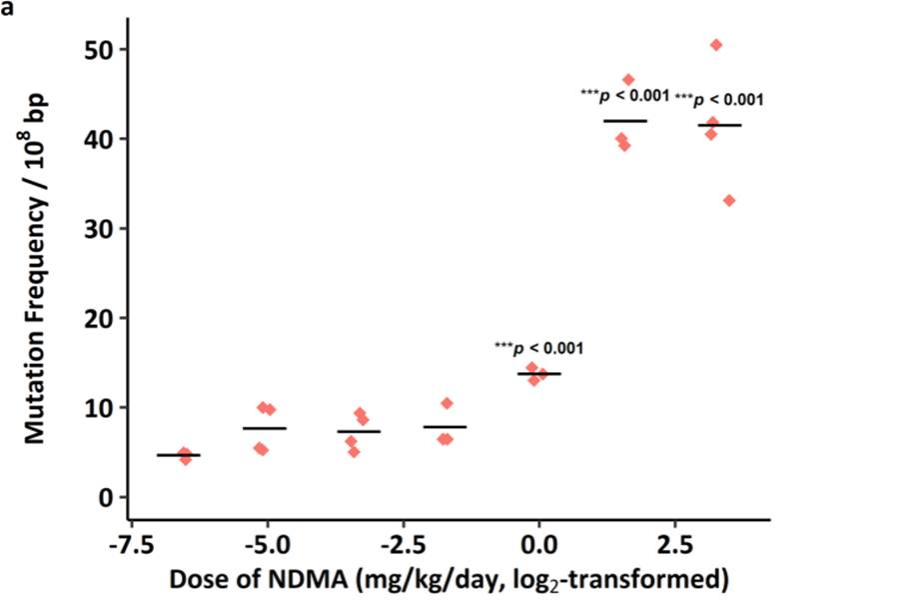
图1. PECC-Seq检测到的NDMA诱导小鼠肝脏突变频率的剂量-反应曲线
创新技术平台PECC-Seq:从方法建立到应用突破
本研究采用的PECC-Seq(Paired-End and Complementary Consensus Sequencing)技术,是团队于2023年在核酸研究领域顶级期刊Nucleic Acids Research(doi: 10.1093/nar/gkad909.)上发表的原创性高通量、高精度突变检测方法。该技术通过对同一DNA双链分子的正反链进行配对一致性测序,将测序错误率降低至10-8以下,实现了全基因组范围内极低频体细胞突变的直接、精准定量。在近期一篇关于ecNGS技术用于监管遗传毒性评估的权威综述中,PECC-Seq被列为核心技术之一。该综述明确指出,ecNGS技术通过直接、高灵敏度地测量突变频率和频谱,解决了传统技术的局限性。文章强调,ecNGS为遗传毒性危害识别和风险评估带来了变革性潜力,其高分辨率数据不仅便于定量分析剂量-反应关系,还能解析突变特征谱,揭示致突变作用模式,从而为监管决策提供更丰富、更可靠的机制性见解。PECC-Seq因其无需外源分子标签、PCR-free建库以及在全基因组SNV检测和突变谱分析方面的有效性被重点介绍。
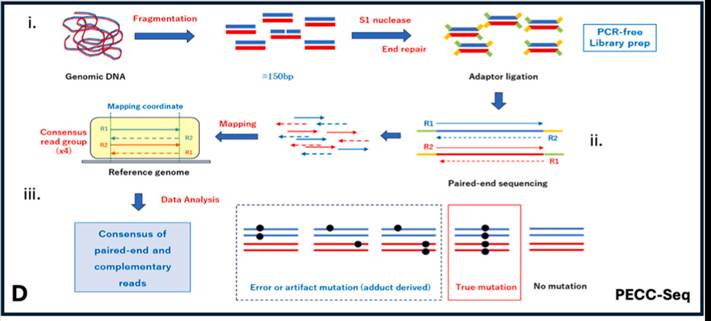
图2. PECC-Seq技术原理示意图 (Regul. Toxicol. Pharm. 164 (2026) 105985)
聚焦NDMA:破解遗传毒性杂质监管难题
NDMA作为最常见的亚硝胺类遗传毒性杂质,近年来在多种药物中被检出,引发全球范围内的药品召回与监管关注。目前,监管机构设定的NDMA每日可接受摄入量(96 ng/天)主要基于啮齿类动物致癌性数据的线性外推,可能无法充分反映其对人体的遗传毒性潜能,且缺乏基于直接突变数据的实验依据。遗传毒性杂质的监管核心在于:在保障用药安全的同时,避免因过于保守的限值导致不必要的药物短缺或研发受阻。因此,建立基于现代分子技术的定量遗传毒性评估体系,为阈值制定提供科学、精准的数据支撑,已成为全球监管科学领域的迫切需求。
本研究通过高精度LC-MS/MS定量NDMA诱导的DNA加合物(N7-Me-Gua和O6-Me-Gua),并利用PECC-Seq检测小鼠肝脏组织中的全基因组体细胞突变。研究发现NDMA诱导的DNA加合物和体细胞突变均呈现剂量依赖性增加,突变频率在≥1 mg/kg/day剂量组出现显著升高。NDMA主要诱导CG>TA和TA>CG碱基转换,其突变谱与COSMIC Signature 11(烷化剂特征)高度相似,从分子机制上印证了其烷化致突变属性。
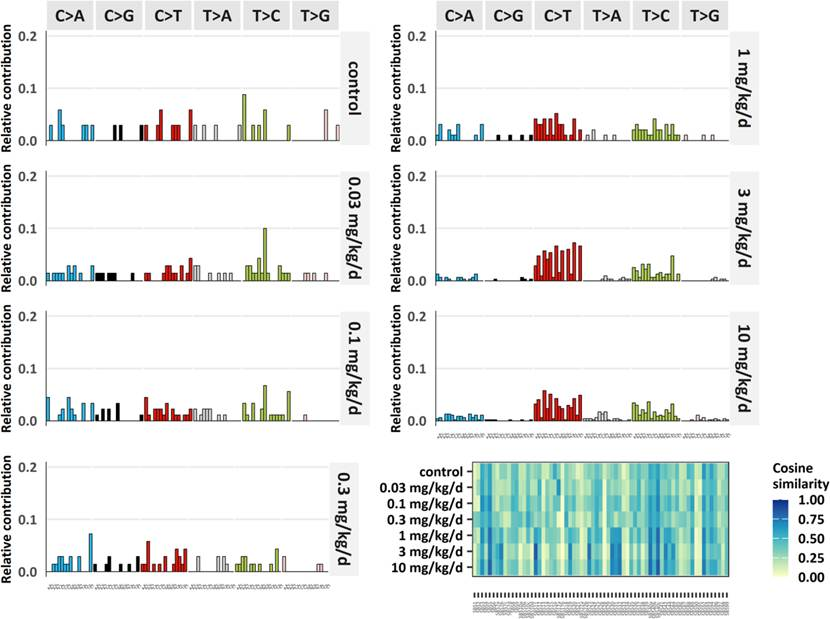
图3. NDMA诱导突变的96种三核苷酸突变谱及其与COSMIC Signature 11的相似性
采用基准剂量(BMD)模型对突变数据进行定量分析,计算得出基于突变终点的BMDL50,并综合考虑物种间、物种内、暴露时长及效应严重性等不确定因子,最终推算出NDMA的突变相关PDE为245 ng/天。该值高于目前监管机构推荐的96 ng/天限值。提示基于致癌性数据的线性外推可能高估了NDMA的致癌风险,而基于直接突变数据的定量评估能为制定更科学、合理的监管阈值提供关键依据。
综上,该研究是PECC-Seq技术创新后的应用案例,提供了一种从DNA损伤到突变固定的完整剂量-反应关系分析框架,能够同时输出突变频率、突变谱和定量阈值三重关键信息,展示了ecNGS技术在遗传毒性定量风险评估和监管决策支持中的巨大潜力。此外,这项工作为亚硝胺类及其他遗传毒性杂质的风险评估范式转变提供了新思路:即从依赖传统、间接的致癌性外推,转向基于高精度、全基因组突变直接检测的定量毒理学评估。随着此类技术在国际遗传毒性测试指南(如OECD)中的逐步认可与标准化,未来有望成为药物杂质管控、化学品安全评价乃至环境健康风险评估中不可或缺的精准工具。
本文通讯作者为上海交通大学医学院公共卫生学院栾洋研究员,团队研究方向见https://www.shsmu.edu.cn/sph/info/1046/1208.htm。上海交通大学医学院的尤馨悦博士与沈阳药科大学的孙琛博士为论文共同第一作者。沈阳药科大学郑江教授团队负责LC-MS/MS DNA加合物定量分析,为本研究提供了关键的早期生物标志物数据。