
2025年12月1日,李巍教授在《美国国家科学院院刊》(PNAS)发表题为《S-cone-specific circuitry in the outer plexiform layer of a cone-dominant mammal》研究成果,结合连续切片扫描电子显微镜(SBEM)、单细胞膜片钳技术、视网膜电图(ERG)和免疫细胞化学等多种形态学和生理学证据,全面解析了十三线地松鼠视网膜外网状层(OPL)中的短波视锥细胞(S-cone)信号传递回路及调控。
短波视锥是哺乳动物视网膜中接收短波长信息(比如蓝光和紫外光)的关键感光细胞,其下游神经回路参与色觉形成和昼夜节律调节等重要视觉信息输入。由于多数模式动物以视杆细胞为主视锥细胞很少,而短波视锥在视锥细胞中占比也很低(~5%),所以其精细结构和功能机制难以解析。十三线地松鼠视网膜以视锥细胞为主,因此成为研究短波视锥生理功能的理想模型。
单个类型的视锥细胞虽然有吸收波峰,但是其输出信号并不能区分光刺激的波长与强度,需下游视网膜回路与其他类型的视锥细胞信号对比整合以产生颜色辨别。从功能上来说,短波通路要完整编码短波/蓝光信号,理论上既需要检测“光出现”的ON通路和检测“光消失”的 OFF通路相互配合。连接短波视锥的ON 型双极细胞(SCBC)是哺乳动物视网膜中进化保守的核心细胞类型,普遍存在于各类哺乳动物中,与之相应,也该存在一种专门接收短波视锥信号的 OFF型双极细胞。但这种细胞是否真的存在,学术界至今没有统一结论;更关键的是,即便在灵长类特有的midget(一对一)通路系统中,不同物种是否存在这类S-OFF细胞也有物种差异。此外,灵长类动物中的Hii 型水平细胞是目前已知唯一具有短波视锥特异性的水平细胞,其核心功能是通过负反馈到短波视锥形成色觉周边抑制,参与S-ON、L/M-OFF 的色觉拮抗。除此之外,在许多物种中,水平细胞的部分亚型还会延伸出一条长长的轴突:它在外网状层内呈横向投射,通常会靶向视杆细胞,但这种特殊轴突的具体生理功能,至今仍未被阐明。
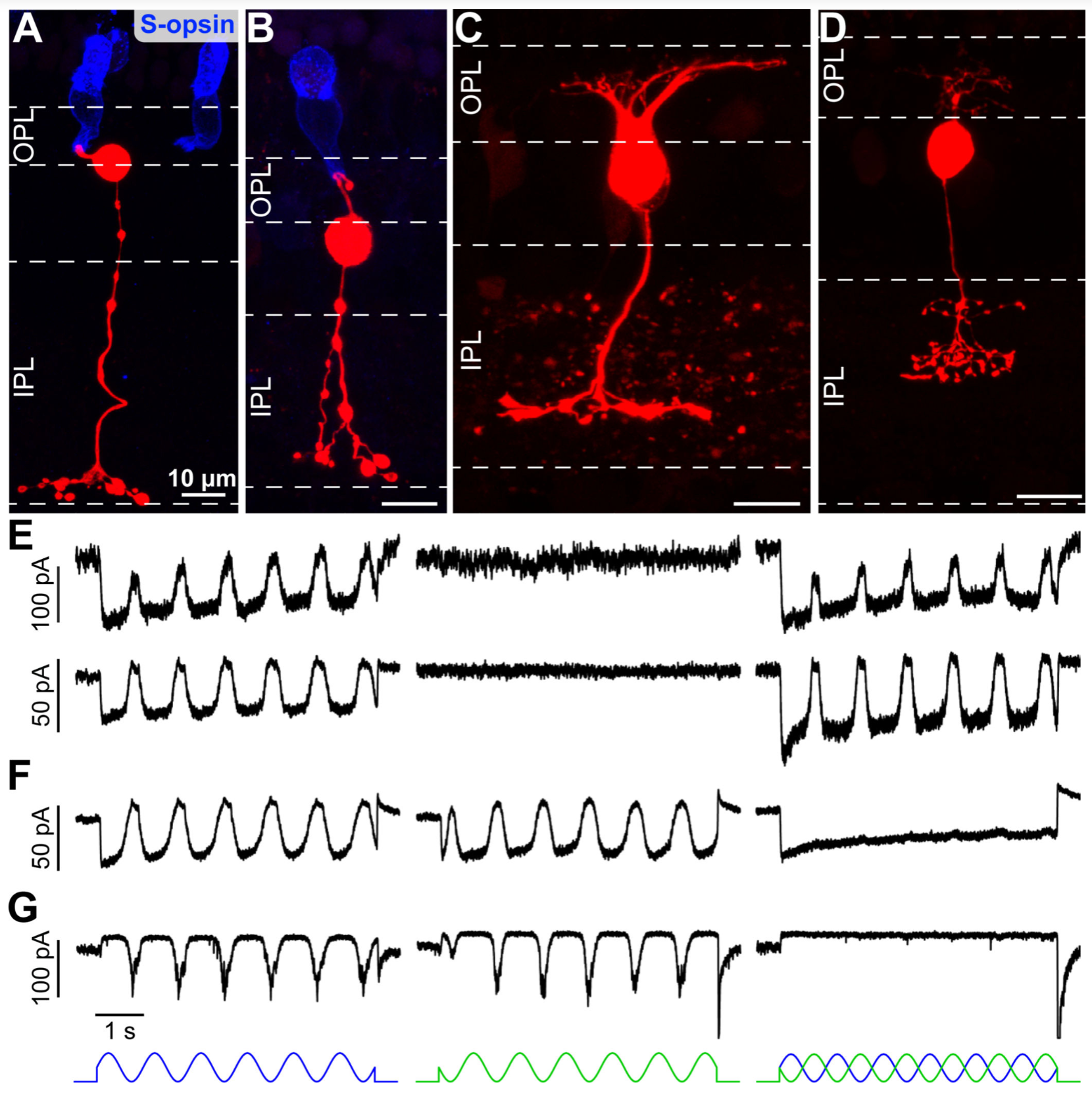
研究团队首先通过 SBEM技术对视网膜外网状层区域进行三维重建,精准识别出 短波视锥细胞及其突触连接,发现该区域仅存在 ON 型双极细胞这一短波视锥特异性双极细胞(SCBC),未观察到特异性S-OFF 型双极细胞的形态学证据;研究团队进一步结合电生理学记录,验证了 SCBC 对蓝光的 ON 极性特异性反应,且未记录到符合 S-OFF 双极细胞特征的光反应;进一步通过长时程ERG 技术,发现在短波视锥特异性刺激下代表 OFF 双极细胞活动的 d 波完全消失,仅有代表 ON 双极细胞活动的 b 波随强度升高而增强。这些检测形态和功能的多角度交叉实验结果明确了十三线地松鼠短波视锥信号仅依赖 ON 型 SCBC 构成的单一通路,进一步验证了李巍团队之前提出的S-OFF 信号可能由中间神经元(无长突细胞)介导的假说 (Chen & Li,Nature Neuroscience, 2012),完善了哺乳动物短波视锥信号传递的基本框架。
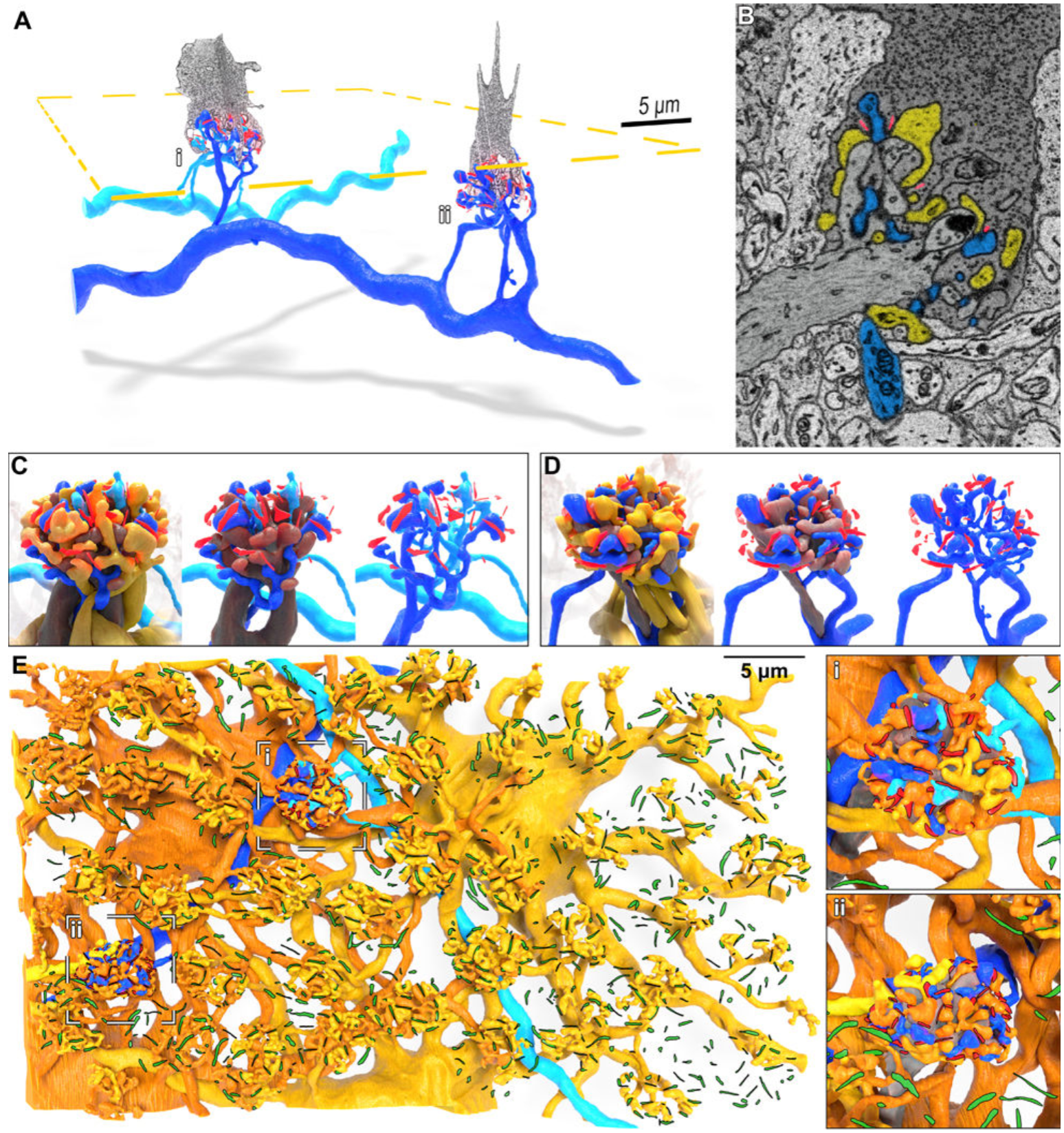
本研究的另一个亮点是发现地松鼠视网膜的两种水平细胞存在严格分工:H2 细胞的树突仅与短波视锥细胞形成突触,专门负责短波视锥信号的侧向抑制,以增强短波长光的对比度;而 H1 细胞的树突虽无选择性地连接所有视锥细胞,但其轴突在外网状层内横向投射,形成之前未被发现的密集侧支网络,且特异性地靶向长波视锥细胞,完全回避短波视锥细胞。这一发现揭示了 S、M 视锥信号的分离式调节机制,解释了为何两种锥细胞网络能独立调制突触敏感性,回应了此前水平细胞在色觉辨别中功能不明的争议。
综合所有研究结果,多手段的解剖学和生理学证据共同证实:十三线地松鼠视网膜 S 视锥回路的核心特征,即仅通过 ON 型双极细胞传递S-ON信号,由 H2 细胞专门调节短波视锥、H1 轴突专门调节长波视锥,形成独立的信号处理通道。这一发现不仅揭示了非灵长类哺乳动物短波视锥回路的典型模式(灵长类动物在此基础上进一步进化出高分辨率色觉回路),更确立了十三线地松鼠作为研究哺乳动物短波视锥回路的理想模型,为理解蓝光对色觉、昼夜节律以及近视形成的影响提供了关键理论支撑。
美国国立卫生研究院国立眼科研究所李巍高级研究员(现任职于上海交通大学医学院尚思神经与视觉研究院)以及李巍在NIH团队的John M Ball博士为本文共同通讯作者。文章的第一作者张艺臻目前是NIH-布朗大学联合培养博士生,曾因本研究的早期工作而获得美国高中生因特尔科技奖并受到美国奥巴马总统的接见。
论文链接:https://www.pnas.org/doi/10.1073/pnas.2504954122
